1.可能用到的相对原子质量:H-1,C-12,N-14,O-16,Cl-35.5
![]()
2.常见金属在溶液中的活动顺序如下:
3.部分酸、碱和盐的溶解性表(室温)
| H+ | NH4+ | K+ | Na+ | Ba2+ | Ca2+ | Mg2+ | Al3+ | Fe3+ | Cu2+ | Ag+ |
OH- |
| 溶、挥 | 溶 | 溶 | 溶 | 微 | 不 | 不 | 不 | 不 | - |
NO3- | 溶、挥 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 |
Cl- | 溶、挥 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 不 |
SO42- | 溶 | 溶 | 溶 | 溶 | 不 | 微 | 溶 | 溶 | 溶 | 溶 | 微 |
CO32- | 溶、挥 | 溶 | 溶 | 溶 | 不 | 不 | 微 | - | - | - | 不 |
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发,“-”表示那种物质不存在或遇到水就分解了。
选择题(共10分)
1.空气中体积分数约为78%的气体是 ( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
2.下列现象中,一定发生化学变化的是 ( )
A.玻璃破碎 B.干冰升华 C.木炭燃烧 D.轮胎爆炸
3.下列物质中,由原子构成的是 ( )
A.水 B.金刚石 C.二氧化碳 D.氢氧化钠
![]()
 4.下列实验操作不正确的是 ( )
4.下列实验操作不正确的是 ( )
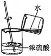
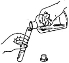
A.取用液体 B.加热液体 C.稀释浓硫酸 D.蒸发食盐水
5.下列说法中错误的是 ( )
A.酒精是一种可再生能源 B.稀盐酸和稀硫酸都可以除铁锈
C.二氧化硫是一种空气污染物 D.食用大量新鲜蔬菜,水果为人体补充维生素
6.下列关于氨气的说法中,正确的是 ( )
A.氨气是一种氧化物 B.氨气中含有3个氨分子
C.氨气中氨、氢元素质量比为17:3 D.氨气的相对分子质量是17
7.下列有关事实的解释中,错误的是 ( )
A.生铁和钢的性能不同——含碳量不同
B.硫和磷的元素种类不同——质子数不同
C.水和过氧化氢的化学性质不同——氧原子个数不同
D.Na和Na+化学性质不同——最外层电子数不同
8.下列说法中,正确的是 ( )
A.Fe和Fe2O3都能与稀盐酸反应,都生成氧化铁
B.置换反应前后一定有化合价发生变化
C.可用酸碱指示剂测定溶液酸碱度
D.生成盐和水的反应一定属于中和反应
9.下列有关实验操作顺序的“先”与“后”的说法中,正确的是 ( )
A.制备气体时,先装药品,后检查装置的气密性
B.用滴管取用细口瓶中的液体时,先将其伸入液体内,后挤压取液
C.用托盘天平称量10g药品时,先放砝码,后放药品
D.加热KMnO4并用排水法收集O2,实验结束时先熄灭酒精灯,后移除导管
10.下列实验方案中正确的是 ( )
A.用稀盐酸除去CaO中的少量CaCO3
B.区分NaOH溶液和NaCl溶液,取样,分别加入水中观察温度变化
C.分离NaCl和CaCO3的混合物,取样,加水溶解再过滤
D.除去铜粉中的铁粉,向化合物中加入足量的稀盐酸,充分反应后,过滤、洗涤、烘干
非选择题(共40分)
11.回答下列问题
⑴ 氢离子的符号是________; ⑵ H2O中氧元素的化合价是________
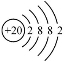
 12.根据右图回答下列问题
12.根据右图回答下列问题
⑴ 钙的相对原子质量为________
⑵ 钙原子在化学反应中易________个电子形成钙离子
⑶ 生石灰是钙的氧化物,请写出它与水反应的化学反
应方程式__________________________
13.回答下列有关水的问题
⑴ 在净水过程中,常利用活性炭的_______性除去异味和有色的物质;
⑵ 日常生活中,可用________区分硬水和软水;
⑶ 正常雨水的pH_______7(选填“>”、“=”或<”)。
14.回答下列生活中与化学有关的问题
⑴ 发酵粉的主要成分为小苏打,其化学式为_______。
⑵ 炒菜时油锅中的油不慎着火,可以采取_____________________的灭火方法。
⑶ 利用厨房中的_______可以溶解水壶中的水垢【主要成分为CaCO3和Mg(OH)2】
15.碳和碳的化合物是自然界中重要的物质,回答下列问题
![]() ⑴ 金刚石、石墨、C60都是碳的单质,完全燃烧时都会生成_______。
⑴ 金刚石、石墨、C60都是碳的单质,完全燃烧时都会生成_______。
![]() ⑵ 在炼铁原理中(3CO+Fe2O3 3CO2+2Fe),发生氧化反应的物质是_______。
⑵ 在炼铁原理中(3CO+Fe2O3 3CO2+2Fe),发生氧化反应的物质是_______。
![]()
![]() ⑶ CO和CO2化学性质不同的原因是______________。
⑶ CO和CO2化学性质不同的原因是______________。
![]()
![]()
![]()
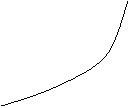
![]() 16.分析甲、乙两种固体的溶解度曲线,回答下列问题。
16.分析甲、乙两种固体的溶解度曲线,回答下列问题。
![]()
![]() ⑴ A点表示_____________________。
⑴ A点表示_____________________。
![]()
![]()
![]()
![]() ⑵ 若B点表示60℃时将40g甲放入100g水中,
⑵ 若B点表示60℃时将40g甲放入100g水中,
![]()
![]()
![]()
![]()
![]()
![]()
![]() 将其变成恰好饱和的溶液的方法之一:__________。
将其变成恰好饱和的溶液的方法之一:__________。
![]()
![]()
![]() ⑶ 若B点表示60℃时乙物质的______________
⑶ 若B点表示60℃时乙物质的______________
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() (填饱和溶液或不饱和溶液),此温度下其溶质的质量
(填饱和溶液或不饱和溶液),此温度下其溶质的质量
分数为_______。(结果保留0.1%)

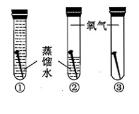
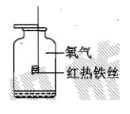 17.下列是研究氧气、铁、二氧化碳的实验。根据图示,回答问题。
17.下列是研究氧气、铁、二氧化碳的实验。根据图示,回答问题。
![]()
![]()
![]()
⑴ A中铁丝在氧气中燃烧,集气瓶底部放少量水,其作用是______________。
⑵ B中实验的目的是_____________________。
⑶ C中观察到的现象是_____________________。
18.化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案
![]()
![]()
![]() ⑴试管乙中观察到的现象是______________,反应的化学方
⑴试管乙中观察到的现象是______________,反应的化学方
![]()
![]()
![]() 程式为_________________________。
程式为_________________________。
⑵ 同学们经讨论后认为该方案可以优化,_______试管
的实验是多余的。
![]()
![]()
![]()


 ⑶ 去除多余的实验,同学们将另两只试管中反应后的物质
⑶ 去除多余的实验,同学们将另两只试管中反应后的物质
倒入同一大烧杯中,一段时间后过滤,向滤渣中加入稀硫酸,
有气泡产生,则滤渣的成分可能是_____________________。(写出所有可能的情况)
19.配制50g质量分数5%的氯化钠溶液,结合实验回答下列问题。
⑴ 配制50g质量分数为5%的氯化钠溶液,需氯化钠_______g。
⑵ 溶解时需要用到的仪器是_____________________。
⑶ 下列操作中,会引起溶质质量分数偏大的是______________。
A.得到的氯化钠未完全干燥 B.用量筒取水时,俯视读数
C.装瓶时洒出少量溶液 D.称量读数时天平指针偏左
20.以下是实验室里制取气体是常用到的部分仪器。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() a b c d e f g h i
a b c d e f g h i
⑴ 在实验室里,利用化学反应2KClO3 2KCl+3O2↑来制取氧气。
①除选用上图中的部分仪器外,还必须补充的玻璃仪器是_______。
②蜡烛燃烧实验中用到的氧气,最好采用____________法收集。
⑵ 用上述部分仪器制取CO2
①选择C的优点是_____________________。
②若要用73g10%的稀盐酸与足量的大理石反应,理论上制取_______gCO2。
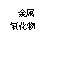
![]() 21.同学们在复习时构建了如图所示的知识网络,“-”表示相连物质在一定条件下可以发生反应。请回答下列问题。
21.同学们在复习时构建了如图所示的知识网络,“-”表示相连物质在一定条件下可以发生反应。请回答下列问题。
![]() ⑴ 若图中M是石蕊溶液,则遇酸溶液显_______色。
⑴ 若图中M是石蕊溶液,则遇酸溶液显_______色。
![]()
![]()
![]() ⑵ Mg、MgO、MgCO3和Mg(OH)2都可以和某物质反应生
⑵ Mg、MgO、MgCO3和Mg(OH)2都可以和某物质反应生
![]()
![]() 成MgCl2,则该物质是_______。
成MgCl2,则该物质是_______。
![]()
![]()
![]()
![]() ⑶ 从图示可知,能与碱发生反应的物质有_______类。
⑶ 从图示可知,能与碱发生反应的物质有_______类。
![]()
![]() ⑷ 根据碱的性质判断,下列实验能够达到目的的是_______。
⑷ 根据碱的性质判断,下列实验能够达到目的的是_______。
![]() A.用CuO和NaOH制取Cu(OH)2
A.用CuO和NaOH制取Cu(OH)2

![]()
![]()
![]()
![]() B.用Ca(OH)2溶液吸收SO2
B.用Ca(OH)2溶液吸收SO2
C.用Ca(OH)2溶液鉴别稀盐酸和NaCl溶液
⑸ 图中有_______条连线间的物质反应一定生成盐和水。


![]()
![]()
![]() 22.某化学兴趣小组设计了一个验证某氯化钠溶液中混有碳酸钠、硫酸钠和氢氧化钠的实验方案,实验流程如图所示:
22.某化学兴趣小组设计了一个验证某氯化钠溶液中混有碳酸钠、硫酸钠和氢氧化钠的实验方案,实验流程如图所示:
⑴ 当测得B中溶液的pH=10时,即可判断![]()
![]() 原溶液中一定
原溶液中一定
![]()
![]()
![]() 混有______________。
混有______________。
![]()
![]()
![]()
![]() ⑵ 向B中加入过量稀盐酸,观察到_____________________时,
⑵ 向B中加入过量稀盐酸,观察到_____________________时,
完成对剩余物质的验证。
⑶ 完成实验后,将C中物质过滤,滤液中一定含有的溶质是______________。
答案
![]() 答案
答案
1.A 2.B 3.B 4.C 5.A 6.D 7.C 8.B 9.C 10.D
11.(1)H+ (2)H2O
12.(1)40.08 (2)失去2 (3)CaO+H2O=Ca(OH)2
13.(1)吸附 (2)肥皂水 (3)<
14.(1)NaHCO3 (2)用锅盖盖灭 (3)食醋
15.(1)CO2 (2)CO (3)分子构成不同
16.(1)在A℃时甲乙两种固体的溶解度相同
(2)加60g甲
(3)不饱和 28.6%
17.(1)防止高温熔化物掉落炸裂瓶底
(2)探究铁生锈条件
(3)烧杯中的蜡烛自上而下依次熄灭
18.(1)有红色固体析出,溶液由红色变为浅绿色 Fe+CuSO4=FeSO4+Cu
(2)丙
(3)Fe、Cu;Mg、Fe、Cu
19.(1)2.5
(2)烧杯、玻璃棒
(3)B、D
20.(1)①试管 ②排空气法
(2)①便于添加液体药品 ②4.4
21.(1)红
(2)HCl
(3)4
(4)B
(5)3
22.(1)NaOH
(2)有气泡产生,部分白色沉淀消失
(3)NaCl 、HCl

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...