![]()

7、生活中的下列变化,属于化学变化的是
A.玉米榨汁 B.葡萄酿酒 C.蔗糖溶解 D.汽油挥发
8、下列关于催化剂的说法正确的是
A.化学反应前后催化剂的质量不变 B.化学反应前后催化剂的性质不变
C.催化剂只能加快化学反应速率 D.没有催化剂化学反应不能发生
9、将密封良好的方便面从襄阳带到西藏时,包装袋鼓起,是因为袋内气体的
A.分子个数增多 B.分子质量增大 C.分子间隔增大 D.分子体积变大
10、一种新型材料C3N4的硬度比金刚石还大,可做切割工具。在C3N4中,C为+4价,则N元素的化合价是
A.+3 B.+1 C.-1 D.-3
11、襄阳市正在创建国家级文明城市。下列做法错误的是
A.加大空气监测力度,改善环境状况 B.有效防治水体污染,保护水资源
C.分类回收生活垃圾,垃圾资源化 D.过度使用农药化肥,提高粮食产量
12、同素异形体是指由同种元素组成的不同单质。下列和氧气互为同素异形体的是
A.臭氧 B.液氧 C.石墨 D.二氧化碳
13、下列说法正确的是
A.由同一种元素组成的物质一定是单质
B.由同种分子构成的物质一定是纯净物
C.蜡烛燃烧后质量减小,不遵守质量守恒定律
D.凡是均一的、稳定的液体一定是溶液
14、下列实验方案不能达到目的的是
A.将气体通过灼热的铜网,除去N2中的少量O2
B.将气体通过装有NaOH溶液的洗气瓶,除去CO中的少量CO2
C.将固体粉末加水溶解、过滤,除去CaO中的CaCO3
D.用点燃的方法鉴别涤纶线与羊毛线
15、下列各组离子能在pH=3的溶液中大量共存的是
A.NH4+、Na+、NO3-、CO32- B. NO3-、Cu2+、SO42-、OH-
C. Mg2+、K+、SO42-、Cl- D.Ca2+、Na+、HCO3-、Cl-
16、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如右图所示。有关该反应过程中的下列说法正确的是
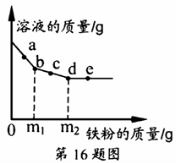
A.a点,向溶液中滴加稀盐酸,无白色沉淀
B.c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生
C.d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2
D.e点,过滤后得到的固体中只含有2种物质
化学部分(共30分)
填空与简答题(每空1分,共16分)
42、生活中处处有化学。请你根据所学的知识,用相应的化学式填空。
(1)按体积计算, 空气中含量最多的气体_______________;
(2)实验室制取氧气的药品_____________ (任意写出一种)。
43、水是生命之源,与人类生活息息相关。
(1)汉江是襄阳的母亲河。汉江水属于_______________ (填“纯净物”或“混合物”)。
(2)饮用硬度过大的水不利于人体健康,生活中常用_________的方法来降低水的硬度。(3用铝制水壶在煤气灶或煤炉上烧水是利用了铝的_________性。
44、学好化学能使我们更科学地认识、分析生活中的各种现象和事物。
(1)襄阳盛产山药、麦冬等经济作物,其中化肥对农作物的增产有重要作用。请你选用N、P、K、O、H等元素,任意写出一种复合肥的化学式:_________________。
(2)古人在野外生火时常“钻木取火”。“钻木取火”满足的燃烧的条件是_________ (填序号)。
A.提供可燃物 B.与氧气接触 C.达到燃烧所需的最低温度
(3)冶金工业常用CO还原CuO来冶炼金属铜,请写出该反应的化学方程式_____________________________。
45、2018年4月7日,我国“深海勇土”号载人潜水器完成运行阶段首航,作业能力达到水下4500米,潜水领域再次获得新突破。
(1)潜水器使用了钛合金等新型合金材料,避免普通的钢铁制品长期使用会生锈。铁生锈的条件是铁与___________直接接触。
(2)潜水器内所用的下列材料属于有机合成材料的一项是_________ (填序号)。
A.不锈钢机械臂 B.有机玻璃仪表盘 C.钢缆绳 D.真皮坐垫
(3)潜水器可用过氧化钠(Na2O2)来供氧。过氧化钠能与人体呼出的二氧化碳反应生成氧气和一种俗名为纯碱的物质,请写出该反应的化学方程式_______________________。
46、A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示,请分析作答:
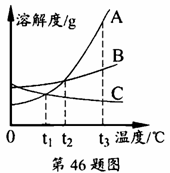
(1)t1℃时,A、C物质的溶解度关系是A___C (填“>”、“=”或“<”);
(2)t3℃时,将A、B、C的饱和溶液各100g,分别降温至t2℃,所得溶液中溶质的质量由大到小依次为_________________。
47、图示中A一F是初中化学常见的物质,其中A是一种钠盐,C、D为氧化物,A、B、C、D、E中都含有氧元素,且物质C的固体俗称“干冰”。图中“—”表示相连的两种物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。请分析后作答:
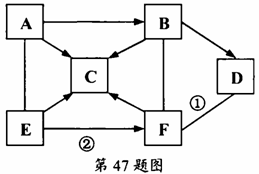
(1)物质C的化学式__________________;
(2)反应①的基本反应类型是__________________;
(3)反应②的化学方程式___________________________________。
实验与探究题(每空1分,共8分)
48、具备基本的化学实验技能是学习化学和进行探究活动的基础和保证。
(1)初中化学实验室常用于量度液体体积的仪器是__________________;
(2)给试管内液体加热时所盛液体体积不得超过试管容积的__________________;
(3)过滤操作中使用的玻璃仪器有__________________(任写一种)。
49、某化学兴趣小组在探究“复分解反应发生的条件”时,选做了如图所示的三个实验:
(提示:BaCl2溶液呈中性,Na2CO3溶液呈碱性。)
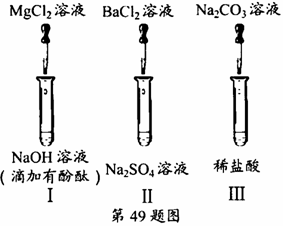
祺祺:向试管I中慢慢滴入MgCl2溶液,并不断振荡,至溶液颜色恰好变为无色为止。请写出该反应的化学方程式_______________________________。
雯雯:分别完成试管II和I中的两个实验后,接着进行如下探究,请分析后作答:

(1)雯雯经过分析推断,试管Ⅲ反应后所得溶液中一定含有的溶质是_______________;步骤①中一定发生的反应的化学方程式是________________________________。
(2)祺祺把沉淀M、N混合后加入AgNO3溶液和过量的稀硝酸,观察到的实验现象是___________________________________;实验结束,祺祺把反应后的混合物与滤液C
全部倒入废液缸中,则废液缸内上层清液中,除酚酞外一定含有的溶质有___________。
分析与计算题(50题2分,51题4分,共6分)
(可能用到的相对原子质量:H-1 O-16 C1-35.5 Ca- 40 Zn-65)
50、10%的CaCl2溶液常用作路面的保湿剂。
(1)CaCl2中Ca、Cl元素的质量比为________________;
(2)要配制200 kg 10%的CaCl2溶液,需要水的质量为_______________kg。
51、某同学将锌和氧化锌的混合物20g放入烧杯中,加入一定质量分数的稀硫酸,测得加入稀硫酸的质量与产生氢气质量的关系如图所示。求:
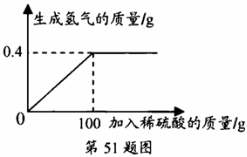
(1)恰好完全反应时生成氢气的质量是_______g;
(2)计算原20g混合物中氧化锌的质量分数。

单项选择题
7-11 BACDD 12-16 ABCCB
填空与简答题
42、(1)N2;(2) KClO3 (或KMnO4、H2O2)。
43、(1)混合物。(2)煮沸。(3)导热。
44、(1)KNO3[或NH4H2PO4、 (NH4)2HPO4、 (NH4)3PO4等, 答案合理即可]。
(2)C。(3)CuO+CO![]() Cu+CO2
Cu+CO2
45、(1)空气中的氧气和水(答案合理即可);
(2)B;
(3)2Na2O2+2CO2=2Na2CO3+O2。
46、(1)=;(2)B>A>C(或“B、A、C”)。
47、(1)CO2;(2)复分解反应;
(3)BaCl2+H2SO4=BaSO4↓+2HCl。
实验与探究题
48、(1)量筒;(2)1/3;(3)玻璃棒(或“烧杯、漏斗”等)。
49、M gCl2+2NaOH=Mg(OH)2↓+ 2NaCl
(1)NaCl、Na2CO3;
BaCl2+Na2CO3= BaCO3↓+2NaCl。
(2)沉淀部分溶解,有气泡产生;
Ba(NO3)2、Mg(NO3)2、 NaNO3、HNO3。
分析与计算题
50、(1)40:71;(2)180。
51、(1)0.4
(2)解:设原20g混合物中锌的质量为x
Zn+H2SO4= ZnSO4+H2↑
65 2
x 0.4g
![]() =
=![]()
x=![]() =13g
=13g
所以原20g混合物中氧化锌的质量分数为:
![]() ×100%=35%
×100%=35%
答:原20g混合物中氧化锌的质量分数为35%。

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...