![]() 2018年曲靖中考化学冲刺试题【精选word版 含答案】
2018年曲靖中考化学冲刺试题【精选word版 含答案】
由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看!
第Ⅰ卷 选择题(共45分)
一、选择题(本大题共20小题,其中第1~15小题,每小题2分。第16~20小题,每小题3分,共45分,每小题只有一个选项符合题意,多选、错选或不选均不得分)
1.下列变化中,属于化学变化的是( )
A.瓷碗破碎 B.干冰升华 C.纸张燃烧 D.石蜡熔化
2.下列物质中,属于纯净物的是( )
A.液氧 B.洁净的空气 C.澄清石灰水 D.钛合金
3.下列实验操作正确的是( )
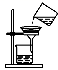
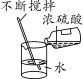
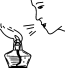
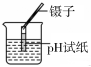
A.过滤 B.稀释浓硫酸 C.熄灭酒精灯 D.测pH
4.下列材料中,属于有机合成材料的是( )
A.钢筋混凝土 B.棉花 C.天然橡胶 D.塑料
5.2022年北京将联合张家口举办冬奥会,下列措施不符合“绿色环保”理念的是( )
A.提倡绿色出行,使用共享单车 B.提倡无纸化办公
C.为营造气氛,大量燃放烟花爆竹 D.加强垃圾的分类回收处理
6.下列有关空气的说法错误的是( )
A.工业上可用分离液态空气的方法制取氧气
B.稀有气体可制成多种用途的电光源
C.二氧化硫、一氧化碳、二氧化氮都属于空气污染物
D.空气的成分按质量计算,氧气约占21%
7.为使植物生长茂盛、叶色浓绿且不易倒伏,下列化肥中最适宜选用的是( )
A.NH4Cl B.KNO3 C.Ca3(PO4)2 D.K2CO3
8.一些食物的近似pH如下,下列说法中不正确的是( )
食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
A.鸡蛋清和牛奶显碱性 B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强 D.胃酸过多的人应少饮苹果汁和葡萄汁
9.下列有关实验现象的描述正确的是( )
A.红磷在空气中燃烧产生大量白色烟雾 B.向稀盐酸中滴加紫色石蕊试液,溶液变蓝
C.硫在氧气中燃烧发出蓝紫色火焰 D.向一定量水中加入氢氧化钠固体,液体温度降低
10.“民以食为天,食以安为先”,下列做法错误的是( )
A.绝对不能食用霉变的花生、大米等食物 B.用甲醛水溶液浸泡海产品,延长保质期
C.用含碳酸氢钠的发酵粉焙制糕点 D.为防止甲状腺肿大,应合理使用加碘食盐
11.下列有关分子、原子的说法正确的是( )
A.热胀冷缩是构成物质微粒的大小随温度的改变而改变的缘故
B.分子是由原子构成的,所以分子一定比原子大
C.分子可以分成原子,而原子不能再分
D.直接构成物质的微粒有分子、原子、离子
12.2017年3·15晚会上曝光了某公司所生产的动物饲料中含有喹乙醇(C12H13N3O4),长期使用会给人类身体健康带来潜在危害。下列关于喹乙醇的说法错误的是( )
A.喹乙醇由碳、氢、氮、氧四种元素组成
B.喹乙醇中氢元素的质量分数最小
C.喹乙醇中碳、氢、氮、氧四种元素的质量比为12∶13∶3∶4
D.喹乙醇的相对分子质量为263
13.雌黄是我国民间早期使用的一种涂改液,其主要成分是三硫化二砷(As2S3),其中硫元素的化合价为-2价,则砷元素的化合价为( )
A.+2 B.+3 C.-3 D.+6
14.
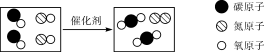
15.如图所示是处理汽车尾气的某化学反应微观示意图,下列说法错误的是( )
A.该反应属于复分解反应
B.该反应中共涉及三种氧化物
C.反应前后原子的种类和数目都不变
D.该反应的化学方程式为2CO+2NO 2CO2+N2
16.下列各组离子在水溶液中能大量共存的是( )
A.H+、NO3-、OH- B.Na+、Ca2+、CO32-
C.OH-、SO42-、Cu2+ D.Ba2+、NO3-、K+
17.下列各组物质的鉴别方法正确的是( )
选项 | 物质 | 鉴别方法 |
A | CO(NH2)2和(NH4)2SO4 | 加熟石灰研磨,闻气味 |
B | CO和CO2 | 闻气味 |
C | K2CO3溶液和K2SO4溶液 | 滴加BaCl2溶液,观察现象 |
D | 黄铜和黄金 | 观察颜色 |
18.归纳推理是学习化学的重要方法之一,下列推理正确的是( )
A.酸雨的pH小于7,故pH小于7的雨水一定是酸雨
B.氧化物中一定含有氧元素,但含有氧元素的物质不一定是氧化物
C.中和反应生成盐和水,故生成盐和水的反应一定是中和反应
D.有机物中一定含有碳元素,故含有碳元素的化合物一定是有机物
19.将一定量的锌粉加入AgNO3和Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液。下列关于滤渣和滤液的分析错误的是( )
A.向滤渣中滴加稀盐酸,若无明显现象,则滤液中一定含有Zn(NO3)2和Cu(NO3)2
B.向滤渣中滴加稀盐酸,若产生气泡,则滤液中一定没有Cu(NO3)2
C.向滤液中滴加稀盐酸,若产生白色沉淀,则滤渣中一定没有Zn和Cu
D.若滤液呈蓝色,则滤渣中一定含有Ag,可能含有Cu
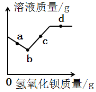
20.常温下,向一定量的碳酸钠溶液中不断加入氢氧化钡粉末,溶液质量的变化情况如图所示。对该图的分析有如下几种说法:
①向a点溶液中滴加无色酚酞溶液,溶液变红,可证明有氢氧化钠生成
②取少量b点溶液,滴入过量稀盐酸,有气泡产生
③c点溶液中的溶质只有氢氧化钠
④该温度下,向d点溶液中加入氢氧化钡粉末,溶质质量不变。
上述四种说法中正确的个数有( )
A.1个 B.2个 C.3个 D.4个
第Ⅱ卷 非选择题(共55分)
二、填空与简答(本大题共5个小题,化学方程式2分,其余每空1分,共33分)
21.(6分)(1)化学用语是学习和研究化学的工具,请用化学用语填空:
①两个汞原子________;②两个铁离子________;③氯气________;
④地壳中含量最高的元素和地壳中含量最高的金属元素组成的化合物的化学式________。
(2)请写出O2中数字的含义:
①“+4”表示________________________;
②“2”表示________________________。
22.(6分)下表是元素周期表的一部分,请回答下列问题。
周期 族 | ⅠA |
| 0 | ||||||
1 | 1 H 氢 1.008 |
| 2 He 氦 4.003 | ||||||
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||||
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 | |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 | |
(1)请画出16号元素的原子结构示意图__________________________。
(2)元素的种类由原子的_____________(填序号)决定。
A.质子数 B.中子数 C.电子数 D.相对原子质量
(3)Na、Mg、Al位于同一周期的原因是________________________________(合理即可)。
(4)请写出与氩原子核外电子排布相同的阴离子的离子符号_________________________(合理即可)。
(5)右图是从元素周期表中截取的一个单元格,你能从该单元格中获取的信息有_________________________________(合理即可)。
![]()
(6)![]() 和
和![]() 所对应元素的化学性质_____________(填“相似”或“不相似”)。
所对应元素的化学性质_____________(填“相似”或“不相似”)。
23.(9分)“科教扶贫”是实施精准扶贫的有效途径之一,请结合相关知识回答下列问题。
(1)提倡绿色发展,开发利用新能源,减少使用煤、石油、__________三大化石燃料。中国地质调查局2017年5月18日宣布,我国成功完成可燃冰的实验开采工作,可燃冰的气体成分主要是甲烷,要使其在空气中燃烧,还需具备的条件是_______________________。其燃烧的化学反应方程式为________________________________________。
(2)倡导科学膳食,注重营养均衡,人类必须摄取的六大基本营养素是糖类、________、油脂、维生素、无机盐和水。其中富含维生素的食物有________________________________________(任写一种)。
(3)注重科学选材,完善基础设施。铁是被广泛使用的一种金属材料,其缺点是易与水和 反应而锈蚀,铁锈可用稀盐酸除去,其反应的化学方程式为 。
24.(7分)水与溶液是生活中常见的化学物质,请结合所学知识回答下列问题。
(1)净化水时,常见活性炭除去水中的异味和色素,是利用了活性炭的___________性。
(2)电解水时,通电一段时间后,负极与正极所产生的气体体积比约为____________,由该实验可知水由______________________组成。
(3)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答下列问题。
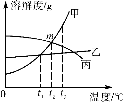
①t3℃时,三种物质的溶解度由大到小的顺序是 。
②交点m表示的含义是 。
③若甲物质中混有少量丙物质,要得到比较纯净的甲物质可采用的方法
是 。
④将t3℃时甲、乙、丙三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数大小关系是 。
25.(5分)A、B、C是初中化学中常见的物质,它们之间的转化关系如图所示:(“―→”表示一种物质可以转化为另一种物质;反应条件、部分反应物和生成物已略去)。
(1)若A、B、C三种物质均含碳元素,其中一种物质是单质,则A物质的化学式为______,B物质的化学性质有_______________________________________(任写一条);实验室检验C物质的化学方程式为______________________________________。
(2)若A、B、C均为金属,则三种金属的活动性顺序由强到弱的顺序是_____________(用A、B、C表示)。

三、实验与探究(本大题共2个小题,化学方程式2分,其余每空1分,共16分)
26.(8分)化学是一门以实验为基础的科学,请结合图示回答问题。
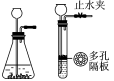
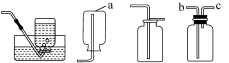
A B C D E F G
(1)图中a仪器的名称是 。
(2)实验室加热高锰酸钾固体制取氧气的化学反应方程式为 。若用G装置收集氧气,气体应从 (选填“b”或“c”)端通入。
(3)实验室常用大理石和稀盐酸反应制取二氧化碳,发生装置最好选用C,与B装置相比,C装置的优点是 ,收集装置可选用D、E、F中的 ,其化学反应方程式为 。
27.(8分)科学探究是学习化学的重要方式,某兴趣小组在做完氯化钡溶液和硫酸钠溶液反应的实验后,欲探究反应后所得溶液中溶质的成分,请你和他们一起完成该探究方案。
(温馨提示:该实验过程中所用溶液的浓度较低,实验中若涉及硫酸钙、氢氧化钙等微溶物,均视为可溶物)
【提出问题】反应后所得溶液中溶质的成分是什么?
【做出猜想】猜想一:NaCl; 猜想二:NaCl和BaCl2;
猜想三:NaCl和Na2SO4; 猜想四:NaCl、BaCl2和Na2SO4。
经过讨论,大家一致认为猜想 不合理,理由是 (用化学方程式表示)。
【设计实验】
(1)取少量反应后的溶液于试管中,向其中加入适量 (任写一种)溶液,若产生白色沉淀,则猜想二成立。
(2)取少量反应后的溶液于试管中,向其中加入适量 (任写一种)溶液,若产生白色沉淀,则猜想三成立。
(3)如果(1)和(2)中均没有产生白色沉淀,则猜想一成立。
【交流反思】小组同学一致认为,探究反应后所得溶液中溶质的成分,除考虑生成的可溶物外,还需要考虑 。
【拓展延伸】某同学提出了以下两种检验溶液中硫酸根离子的方法:
方法一:取少许待测液,先滴加氯化钡溶液,若产生白色沉淀,继续滴加足量稀盐酸,振荡,沉淀不溶解,则待测液中一定含有SO42-。
方法二:取少许待测液,先滴加足量稀盐酸,若无明显现象,继续滴加氯化钡溶液,产生白色沉淀,则待测液中一定含有SO42-。
上述两种方法中,方法 合理,另一种方法不合理的理由是待测液中若含有 (填离子符号),也会产生相同的现象,从而得出错误的结论。
四、计算与分析(本大题共1个小题,共6分)
28.(6分)现有一瓶贴有如下标签的氯化钠溶液,为检测该溶液的实际浓度与所贴标签上的浓度是否相符,取该氯化钠溶液10 g,向其中加入10 g溶质质量分数为3.4%的硝酸银溶液,恰好完全反应。请计算并回答问题。
(温馨提示:化学反应方程式为NaCl+AgNO3===AgCl↓+NaNO3,该题中的“浓度”指溶质质量分数。)
(1)该氯化钠溶液的实际浓度与所贴标签上的浓度 (填“相符”或“不相符”)。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(计算结果保留到0.1%)

![]() 2018年曲靖中考化学冲刺试题参考答案
2018年曲靖中考化学冲刺试题参考答案
一、选择题
1~5:CABDC 6~10:DBACB 11~15:DCB A 16~20:DABAA
二、填空与简答
21.(1)①2Hg ②2Fe3+ ③Cl2 ④Al2O3 (2)①二氧化碳中碳元素的化合价为+4价
②一个二氧化碳分子中含有2个氧原子
22.(1)![]() (2)A (3)它们原子的核外电子层数相同 (4)Cl-(或S2-、P3-) (5)氢的相对原子质量为1.008(合理即可) (6)不相似
(2)A (3)它们原子的核外电子层数相同 (4)Cl-(或S2-、P3-) (5)氢的相对原子质量为1.008(合理即可) (6)不相似
23.(1)天然气 温度达到着火点 CH4 +2O2 CO2 +2H2O (2)蛋白质 青菜(或西红柿、苹果等水果或蔬菜) (3)氧气 Fe2O3+6HCl=== 2FeCl3+3H2O
24.(1)吸附 (2)2∶1 氢元素和氧元素 (3)①甲>丙>乙 ②t2℃时甲和丙的溶解度相等
③降温结晶 ④丙>甲=乙
25.(1)CO 常温下化学性质稳定(或还原性,可燃性等) Ca(OH)2+CO2===CaCO3↓+H2O
(2)C<A<B
三、实验与探究
26.(1)集气瓶 (2)2KMnO4 K2MnO4 + MnO2 + O2↑ b (3)可以控制反应的发生和停止
F CaCO3+2HCl===CaCl2+H2O+CO2↑
27.四 BaCl2+Na2SO4===2NaCl+BaSO4↓ (1)稀硫酸(或可溶性硫酸盐或可溶性碳酸盐)
(2)BaCl2[Ba(NO3)2或Ba(OH)2] 可溶性的反应物是否过量 二 Ag+
四、计算分析题
28.(1)不相等
(2)解:设10g氯化钠溶液中含氯化钠的质量为x,恰好完全反应时生成氯化钠的质量为y,硝酸钠的
质量为z
NaCl + AgNO3 === AgCl↓+NaNO3
58.5 170 143.5 85
x 10g×3.4% y z
= x=0.117 g
= y=0.287 g
= z=0.17 g
反应后所得溶液的溶质质量分数=×100%≈0.9%
答:(1)氯化钠溶液中溶质的质量分数=×100%=1.17%>0.9%,该氢氧化钠溶液的实际浓度与所贴标签上的浓度不相符;(2)恰好完全反应时所得溶液中溶质的质量分数约为0.9%。

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...