2018重庆实验外国语学校中考化学模拟试题【精编Word版】
由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看!
相对原子质量:H-1 O-16 C-12 Na-23 S-32 C1-35.5 Ca-40 Fe-56 Cu64 Ba-13
一、选择题(本题共16个小题,每小题只有1个选项符合题意,每小题2分,共32分)
1.下列是化学变化的是( )
A.霓虹灯发光 B.二氧化碳使润湿的石蕊试纸变红
C.蜡烛熔化 D.工业制取氧气
2.青少年正是长身体的时期,饮食既要均衡、适量,又要注意卫生、安全。下列说法正确是( )
A.霉变食物洗净后食用 B.用甲醛溶液保鲜食物
C.食盐加碘可防贫血 D.多吃水果补充维生素
3.今年4月22日是第49个世界地球日,主题是“珍惜自然资源呵护美丽国土—讲好我们的地球故事”。下列做法不应该提倡的是( )
A.生活垃圾分类回收,合理利用 B.回收废旧电池,节约金属资源
C.经常使用一次性筷子,塑料袋等 D.开发太阳能、风能等,减少对化石能源的依赖
4.下列有关氧气的说法,正确的是( )
A.用燃烧法测定空气中氧气含量,可用铁丝替代红磷
B.氧气约占空气总质量分数的21%
C.鱼能在水中生活,证明氧气易溶于水
D.用带火星的木条是否复燃来检验氧气
5.水与人们的生产生活息息相关,下列有关水的说法不正确的是( )
A.为了保护水资源,禁止使用化肥和农药
B.活性炭可吸附水中的色素和异味
C.蒸馏可使海水淡化
D.肥皂水鉴别硬水和软水
6.下列化学符号表示两个分子的是( )
A.![]() B.
B.![]() C.2Fe D.
C.2Fe D.![]()
7.下列物质不属于溶液的是( )
A.果粒橙 B.可乐 C.白醋 D.碘酒
8.2017年12月6日,重庆到西安的高铁正式开通,极大方便了市民出行,建设中用到:
![]() 对钢轨中的缝隙进行焊接,该反应中发生氧化反应的物质是( )
对钢轨中的缝隙进行焊接,该反应中发生氧化反应的物质是( )
A.![]() B.Al C.
B.Al C.![]() D.Fe
D.Fe
9.化学肥料和农药对农业的高产丰收具有重要作用,下列有关说法不正确的是( )
A.![]() 是复合肥料
是复合肥料
B.熟石灰可用于改良酸性土壤
C.观察颜色可区别氯化钾与磷矿粉
D.玉米倒伏是因为缺弹
10.化学世界绚丽多彩,下列实验中有关颜色的描述正确的是( )
A.硫在空气中燃烧出现蓝紫色火焰
B.向氢氧化钠中滴加硫酸铜产生蓝色沉淀
C.镁在空气中燃烧产生耀眼的红光
D.实验室用一氧化碳还原氧化铁产生银白色固体
11.![]() 是重要的资源,以其为原料可获得下列四种物质,下列说法不正确的是( )
是重要的资源,以其为原料可获得下列四种物质,下列说法不正确的是( )
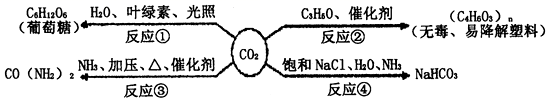
A.反应①是太阳能转化为化学能
B.反应②的实现有利于缓解“白色污染”
C.反应③的产品是复合肥
D.反应④获得的产物还有![]()
12.实验方法多种多样,下列方法能达到实验目的的是( )
A.区分纯铜与黄铜-----看颜色
B.除去二氧化碳中的少量氯化氢-----用氢氧化钠溶液
C.鉴别尿素与氯化钾-------加熟石灰后研磨
D.鉴别稀盐酸和食盐水------用酚酞溶液
13.电解食盐水的化学原理:![]() 。电解一定质量稀食盐水的过程中,下列说法不正确的是( )
。电解一定质量稀食盐水的过程中,下列说法不正确的是( )
A.X的化学式为![]() B.溶液的pH增大
B.溶液的pH增大
C.溶液的质量变大 D.溶液中氢、氧元素的质量比变小
14.在化学实验中关注“气泡”情况很重要,下列说法不正确的是( )
A.检查装置气密性:导管伸入水中,手握容器外壁,有气泡冒出,则装置气密性良好
B.复分解反应的条件之一:生成物中有气体(气泡)生成
C.排水集气法:当导管口的气泡连续均匀时,再开始收集
D.检验氢氧化钠是否变质:向样品溶液中滴加少量的稀盐酸,没有看到气泡,则氢氧化钠没有变质
15.如图是对四个实验绘制的图形,其中实验结果与对应图形正确的是( )
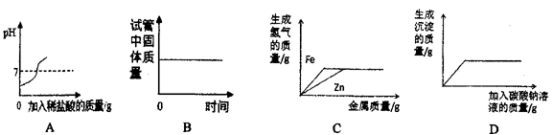
A.向pH=13的氢氧化钠溶液中加入稀盐酸
B.试管中加热高锰酸钾
C.足量的锌粉和铁粉与一定量的稀硫酸反应
D.向含有![]() 和
和![]() 的溶液中加入
的溶液中加入![]() 溶液
溶液
16.某废液中只含有![]() 、
、![]() 、
、![]() 三种溶质。为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量)。下列判断不正确的是( )
三种溶质。为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量)。下列判断不正确的是( )
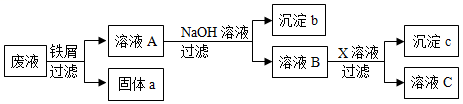
A.固体a是混合物 B.溶液B中的含有的盐是![]() 和
和![]()
C.X可能是![]() D.若回收到6.4g固体a,则加入的铁屑质量为5.6g
D.若回收到6.4g固体a,则加入的铁屑质量为5.6g
二、填空题(本题共5个小题,共20分)
17、(3分)请用适当的化学用语填空:
(1)工业用盐中含有![]() ,在
,在![]() 中氮元素的化合价是__________.
中氮元素的化合价是__________.
(2)钒被誉为“合金中的维生素”。钒元素的部分信息如图所示,钒离子的化学式为________.

(3)新鲜茶叶中含维生素C,其化学式是![]() ,质量分数最大的元素是________.
,质量分数最大的元素是________.
18.(4分)航空航天领域关键技术的突破都离不开航空、航天材料的支撑。下图是一架飞机的模型,回答下列问题:

(1)属于有机合成材料的是____________.
(2)铝具有良好好的抗腐蚀性,其原因是____________________(结合化学方程式解释).
(3)金属钛(Ti)因为有神奇的性能越来越引起人们的关注,钛是航空、军工、电力等领域的重要的原材料。目前大规模生产钛的流程如图所示:
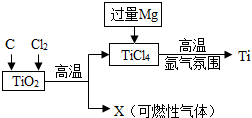
在氨气的气流中,高温下用过量的Mg和![]() 发生置换反应制得钛。写出此反应的化学方程式_______________________________,该过程中氬气的作用:____________.
发生置换反应制得钛。写出此反应的化学方程式_______________________________,该过程中氬气的作用:____________.
19.(4分)40℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发等质量的水,将温度降到30℃,固体溶解情况如图1所示。图2为a、b、c三种物质的溶解度曲线。
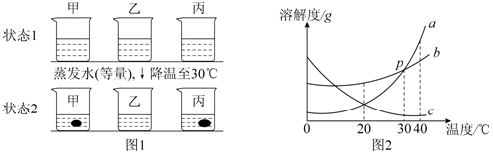
仔细读图1和图2,回答下列问题:
(1)图2中P点的意义是______________________________.
(2)三种物质溶解度的关系:若b>a>c时的温度为t,则t的取值范围是___________.
(3)烧杯甲里是________物质的溶液(填“a”、“b”或“c”).
(4)40℃时,烧杯______里溶液中水的质量最少(填“甲”、“乙”或“丙”).
20.(4分)小明进行了以下活动。

(1)活动1:点燃蜡烛后,电子称示数逐渐减小。蜡烛减小的质量____(填“大于”、·等事”或小于)燃烧后生成物的总量.
(2)活动2:加入泡腾户片(主要成分含柠檬酸、碳酸氢钠等),观察到水中产生大量气泡,蜡烛逐渐熄灭。产生上述现象的原因是________________.
(3)活动3:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中。下列说法正确的__(填序号).
A.可观察到蜡烛熄灭
B.最终杯中液面高于碗中液面
C.该方法能准确测定空气中氧气的含量
(4)活动4:将注射器中浓石灰水注入瓶中,会看到鸡蛋被“吞”入瓶中,该实验中涉及的化学方程式为:____________________.
21.(5分)过氧化钙(![]() )难溶于水,常温下稳定,在潮漫空气及水中缓慢放出氧气,广泛应用于渔业等领域。下图是以大理石(含杂质
)难溶于水,常温下稳定,在潮漫空气及水中缓慢放出氧气,广泛应用于渔业等领域。下图是以大理石(含杂质![]() )等为原料制取
)等为原料制取![]() 的流程图:
的流程图:
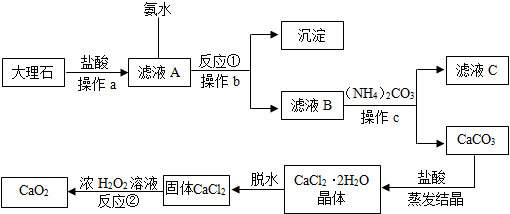
(1)操作a的名称是_______________;
(2)从滤液C中可回收的副产品的化学式为__________;
(3)写出反应①的化学方程式______________________________________;
(4)反应②的基本反应类型是__________________;
(5)在该生产过程中,用110kg大理石制得了72kg的过氧化钙。如果不考虑过程中的损耗,可计算出大理石中![]() 的质量分数为________(结果保留一位小数).
的质量分数为________(结果保留一位小数).
三、实验题(本题共2个小题,共11分)
22、(5分)实验室常用下列装置来制取气体:

(1)写出图中有标号仪器的名称:m__________.
(2)实验室制取二氧化碳可选用的发生装置是____(填序号),若用该发生装置制取氧气的化学方程式为__________________________________.
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。已知常温下![]() 是一种无色、有刺激性气味的气体,密度比空气小,
是一种无色、有刺激性气味的气体,密度比空气小,![]() 极易溶于水,制取并收集
极易溶于水,制取并收集![]() ,应该从上图中选择的制取装置是____________(填序号);
,应该从上图中选择的制取装置是____________(填序号);
(4)若将F装置中的氧气从瓶内排出,水应从____________(填“a”或"b)通入.
3.(6分)东东、西西二位同学为探究盐酸的化学性质,做了如下实验:
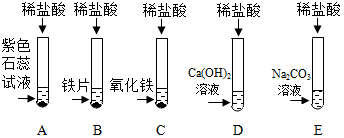
(1)试管A中的现象是_________________,试管B中反应的化学方程式为____________。
(2)反应后试管C中一定有的阳离子是___________(写离子符号).
(3)东东同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成。生成白色沉淀的反应方程式是____________________.
(4)过滤,得到白色沉淀和无色滤液。西西同学欲探究无色滤液中的溶质成分
【提出问题】无色滤液的溶质是什么?
【作出猜想】①![]() ;②
;②![]() ;③
;③![]() ④
④![]()
东东认为猜想________一定不正确(填序号).
【进行实验】

四、计算题(本题共1个小题,共7分)
24.学习小组测定某工业废水(含有![]() )中
)中![]() 的含量。取一定量废水于烧杯中,逐渐加入
的含量。取一定量废水于烧杯中,逐渐加入![]() 溶液,如图所示(过滤后滤液的损失忽略不计):
溶液,如图所示(过滤后滤液的损失忽略不计):
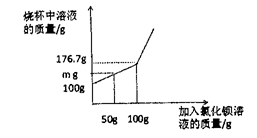
(1)当氯化钡溶液加入50g时,烧杯中溶液的质量m为_______g;
(2)该工业废水中硫酸的质量分数为多少?(写出计算过程)
(3)为避免工业废水污染环境,排放前应处理。如果处理5000g该废水,需加入氧化钙的质量是多少克?

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...