2018开封中考化学模拟真题考试【最新Word版整理含答案】
由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看!
注意事项:
1.本试卷共4页,四个大题,25个小题,满分50分,考试时间50分钟。
2.本试卷上不要答题,请按答题卡上注意事项的要求直接把答案填写在答题卡上,答在试卷上的答案无效。
相对原子质量H:1 C:12 O:16 Na:23 S:32 Cu:64 Zn:65 Ag:108
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
1.下列图标中,表示“禁止烟火”的是

A B C D
2.下列变化属于物理变化的是
A.高梁酿酒 B.干冰升华 C.钢铁生锈 D.纸张燃烧
3.共享单车大大方便了人们的出行。下列自行车所用材料不属于有机合成材料的是
A.合金车架 B.尼龙护套 C.塑料把手 D.橡胶轮胎
4.宏观辨识与微观探析是化学思维方法。下列对宏观事实的微观解释,不正确的是
A.八月桂花飘香——分子在不断地运动
B.中和反应有水生成——H+和OH–结合成水分子
C.电解水生成氢气和氧气——水中含有氢分子和氧分子
D.硫在氧气中燃烧比空气中更剧烈——在氧气中硫接触到的氧分子更多
5.下列图示操作中错误的是
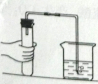
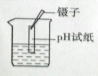

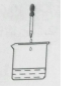
A.气密性检查 B.pH测定 C.浓硫酸稀释 D.滴加液体
6.水是人类生命活动的必需物质。下列说法或做法不正确的是
A.生活污水集中处理后再排放 B.用肥皂水可以鉴别硬水和软水
C.地球上的淡水资源是有限的 D.用活性炭可以将自来水变为纯净水
7.下列河南特产中富含的营养素与其他选项不相同的是
A.灵宝苹果 B.新郑大枣 C.温县山药 D.百泉山楂
8.下列说法不正确的是
A.医疗上硫酸钡可用作钡餐透视 B.施用化肥和农药是作物增产的重要途径
C.氯化钠可用作调味品和防腐剂 D.钙元素是维持生命活动所必需的微量元素
9.工业上可利用钛酸亚铁(FeTiO3)通过两步反应制得钛:
①2FeTiO3+6C+7Cl2![]() 2FeCl3+2TiCl4+6X,②2Mg+TiCl
2FeCl3+2TiCl4+6X,②2Mg+TiCl![]() 2MgCl2+Ti。下列有关说法不正确的是
2MgCl2+Ti。下列有关说法不正确的是
A.X的化学式为CO B.反应①属于复分解反应
C.反应②属于置换反应 D.反应①②均有元素化合价的变化
10.分类法是化学研究的重要方法。下列有关物质的分类正确的是
A.碱:纯碱、烧碱 B.氧化物:生石灰、熟石灰
C.合成材料:塑料、羊毛 D.有机化合物:甲烷、葡萄糖
11.用熟石灰可以鉴别下列各组物质的是
A.KCl和NaCl B.NH4NO3和KNO3 C.CaCl2和Ca(NO3)2 D.NaNO3和CO(NH2)2
12.下列各组物质在水溶液中能大量共存的是
A.NH4Cl、K2CO3、NaOH B.HCl、Na2SO4、KOH
C.BaCl2、KCl、CuSO4 D.K2S04、NH4HCO3、NaCl
13.下列图象分别与选项中的操作相对应,其中不合理的是
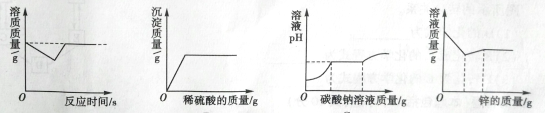
A B C D
A.向一定量的饱和石灰水中加入生石灰
B.向硝酸钡和氢氧化钾的混合溶液中滴加稀硫酸
C.向一定量氯化钙和盐酸的混合溶液中滴加碳酸钠溶液
D.向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入锌粉
14.向盛有5g某黄铜(铜锌合金)样品的烧杯中加入100g稀硫酸,恰好完全反应,反应结束后,测得烧杯内物质的总质量为104.96g。则该合金样品中锌的质量分数是
A.26% B.36% C.63% D.74%
二、填空题(本题包括6个小题,每空1分,共16分)
15.C、H、O、N等元素与人类生活有密切关系,选用其中部分元素组成的化学式进行填空:空气中含量最多的气体是__________;保持酒精化学性质的最小粒子是__________;过量排放会加剧温室效应的氧化物是__________。
16.右图是某品牌矿泉水的标签,标签中钙、镁和钾指的是__________
(填“分子”“原子”或“元素”);偏硅酸(H2Si03)中硅元素的
化合为__________其中氢、氧元素质量比为__________。
17.甲、乙、丙三种固体物质的溶解度曲线如右图所示。
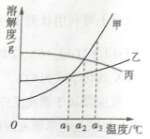
(1)a3℃时,三种物质的溶解度由大到小的顺序是__________;
(2)a3℃时,甲、乙、丙的饱和溶液分别降温到a2℃,溶液中溶质的
质量分数最大的是__________;
(3)甲中混有少量乙,提纯甲的适宜方法为__________。
18.若要验证Fe、Cu和Al的金属活动性顺序,只需一种试剂直
接与上述三种金属反应就能达到目的,该试剂为__________ ;有关反应的化学方程式为__________ 。
19.下图是某反应的微观示意图。
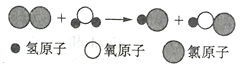
(1)该反应中属于单质的是__________。
(2)已知HClO和碱发生中和反应,则氯气和氢氧化钙发生反应的化学方程式为__________。
20.A、B、C、D、E、F分别为氧气、水、二氧化碳、氢氧化钙、碳酸钠、碳酸钙六种物质中的一种。A可供给呼吸,C俗称熟石灰,它们之间有如右图所示的转化关系。
(1)D的化学式为__________。
(2)B转化成C的化学方程式为__________ 。
(3)F转化成E的化学方程式为__________ 。
三、简答题(本题包括4个小题,共10分)
21.(2分)据报道,今年4月某废品站员工在切割废弃油桶时突然发生爆燃事故,造成严身体伤害。请从爆炸条件的角度分析事故发生的主要原因。
(1)飞机上的镀铬铁制品能防锈蚀,其防锈蚀原理是阻止铁与
__________接触。
(2)设计对比实验是化学研究常用的方法,右图是某化学小组设计
的探究铁钉锈蚀条件的实验。要达到实验目的还需补充什么实验?
23.(3分)为除去粗盐中的CaCl2、MgCl2、Na2S04等可溶性杂质,依次进行了如操作:①溶解;②依次加入过量的BaCl2,,NaOH、Na2CO3溶液:③过滤;④加适量盐酸;⑤蒸发结晶。
(1)上述过程中存在多个复分解反应,其中生成水的有_________个。
(2)加入Na2CO3溶液的作用是什么?
(3)操作③得到固体的成分有哪些?(写出化学式)
24.(3分)某化学兴趣小组设计了如右图所示的微型实验。
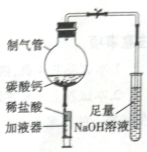
(1)在制气管中加入碳酸钙,推压加液器活塞加入适量稀盐酸,
请用化学方程式表示其反应原理。
(2)当制气管中的反应停止后,试管中溶液倒吸进制气管中,
产生白色沉淀,请解释产生上述现象可能的原因。
四、综合应用题(共10分)
25.钠元素及其化合物是化学研究的重要内容,含钠化合物在社会生产发展中着重要的作用。
(1)下列是钠元素、氯元素在元素周期表中的信息及有关粒子的结构示意图。
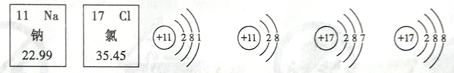
A B C D E F
①D所表示的粒子是_________(填化学符号),氯原子的结构示意图是_________(填字母)。
②D、F形成化合物的化学式是__________。
(2)配制一瓶右图所示溶液需氯化钠__________g;
若配制所得的氯化钠溶液的质量分数偏小,其原因可能
是什么?(写出一条即可)
(3)某化学小组的同学在收集满CO2的集气瓶中放入燃烧的钠,钠继续燃烧,充分反应后生成黑色的碳单质和一种白色固体。推测白色固体的成分可能有三种情况:甲、氧化钠;乙、碳酸钠;丙、氧化钠和碳酸的混合物。
①请设计实验方案证明乙是正确的,而甲和丙均不正确。(提示:氧化钠为白色粉末,溶于水生成氢氧化钠;碳酸钠溶液呈碱性。)
②写出钠在二氧化碳中燃烧的化学方程式。
(4)若将10.6g久置于空气中的氢氧化钠固体样品加入足量的稀硫酸,产生CO2气体2.2g。请计算样品中碳酸钠的质量分数。
2018开封中考化学模拟真题考试参考答案
一、选择题(每小题1分,共14分)
1.D 2.B 3.A 4.C 5.B 6.D 7.C 8.D 9.B 10.D 11.B
12.D 13.A 14.A
二、填空题(每空1分,共16分)
15.N2 C2H5OH CO2
16.元素 +4 1:24
17.(1)甲>丙>乙 (2)甲 (3)冷却热饱和溶液
18.硫酸亚铁溶液 2Al+3FeSO4 ===== Al2(SO4)3+3Fe
19.(1)氯气(或Cl2) (2)2Cl2+2Ca(OH)2 ===== CaCl2+Ca(Cl0)2+2H20
20.(1)CaCO3 (2)Ca0+H 20 ===== Ca(OH)2 (3)2NaOH+C02 ===== Na2CO3+H20
三、简答题(共10分)
21.油属于可燃物,与空气接触,遇明火或温度达到着火点发生燃烧(1分);在有限空间内,气体迅速膨胀,发生爆炸事故(1分)。
22.(l)氧气和水(l分)
(2)补充铁钉在干燥的空气中不发生锈蚀的实验。(1分)
23.(l)2 (1分)
(2)除去CaCl2和过量的BaCl2。(1分)
(3)CaCO3、BaCO3、Mg(OH)2、BaS04。(1分)
24.(1)CaCO3+2HCl ===== CaCl2+H20+CO2↑(1分)
(2)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,装置内气压减小(1分),使试管中液体进入制气管;碳酸钠与氯化钙反应生成难溶于水的碳酸钙(1分。(或2NaOH+C02 ===== Na2CO3+H20,CaCl2+Na2CO3 ===== CaCO3↓+2NaCl。或向下抽拉加液器活塞,装置内气压减小,使试管中液体进入制气管;二氧化碳与氢氧化钠溶液反应生成的碳酸钠与氯化钙反应生成难溶于水的碳酸钙。)
四、综合应用题(共10分)
25.(l)①Na+(l分) E(1分) ②NaCl(1分)
(2)4.5(1分) 用量筒量取水时仰视读数(或转移已称好的氯化钠固体时,部分洒落在烧杯外)(1分)
(3)①取少量该样品溶于水,先加入足量的CaCl2溶液(或BaCl2溶液),出现白色沉淀,过滤,向滤液中滴加酚酞溶液,无明显现象,可证明乙正确,甲和丙均不正确。(l分)
②4Na+3C02![]() 2Na2C03+C (1分)
2Na2C03+C (1分)
(4)解:设碳酸钠的质量为x。
Na2C03+H2S04 ===== Na2S04+H2O+CO2↑(1分)
106 44
x 2.2g
![]() (1分)
(1分)
x=5.3g
质量分数为![]() (1分)
(1分)

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...