![]() 2018年赣州市初三化学联考试题【精编版含答案】
2018年赣州市初三化学联考试题【精编版含答案】
为了方便您的阅读请点击全屏查看
命题人:赖秋霞 王文虎
说明:1.本卷共有五大题,24小题。全卷满分100分,考试时间为70分钟。
2.本卷可能用到的相对原子质量:H-1 C-12 N-14 O-16 P-31 Cl-35.5 Ca-40
3.本卷分为试题卷和答题卷,答案要求写在答题卷上,写在试题卷上不得分。
一、单项选择题(本大题包括10小题,每小题2分,共20分。每小题有四个选项,其中只有一个选项符合题意,请将符合题意的选项代号填在答题卷的相应位置上)
1.下列与“棉”有关的过程中发生了化学变化的是![]() ( )
( )
A. 棉花纺线 B. 棉线织布 C. 棉布制衣 D. 棉衣着火
2.地壳中含量最多的元素是 ( )
A.氧 B.硅 C.铝 D.钙
3.下列物质中,属于纯净物的是 ( )
A.生理盐水 B.高锰酸钾 C.富氧空气 D.乙醇汽油
4.钇元素(Y)是一种稀土元素。磷钇矿是稀土矿的主要矿物之一,其主要成分磷酸钇(YPO4)中磷元素为+5价,则钇元素的化合价为 ( )
A.+1 B.+2 C.+3 D.+4
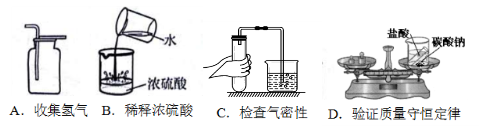
5.下图是初中化学常见的实验操作,其中正确的是 ( )
6.如图是某化学反应的微观示意图,图中不同的圆球代表不同的原子。下列叙述正确的是 ( )
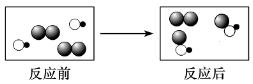
A.该反应的生成物有2种
B.该反应的基本类型是化合反应
C.反应前后分子种类和原子种类均不变
D.参加反应的两种物质的分子个数比为1∶1
7.2018年央视“3·15”晚会发布预警,电动车过充易引发火灾。已知电动车铅蓄电池充电时反应的化学方程式为2PbSO4 + 2H2O = Pb + PbO2+ 2X,则X的化学式为 ( )
A.SO2 B.SO3 C.H2SO3 ![]() D.H2SO4 .
D.H2SO4 .
8.逻辑推理是一种重要的化学思维方法,以下推理正确的是 ( )
A.酸性溶液能使紫色石蕊变红,能使紫色石蕊变红的一定是酸性溶液
B.酸雨的pH小于7,pH小于7的雨水都属于酸雨
C.阳离子都是带正电荷的粒子,带正电荷的粒子一定是阳离子
D.中和反应生成盐和水,生成盐和水的反应都属于中和反应
9.除去下列物质中含有的少量杂质,所用试剂或方法正确的是 ( )
序号 | 混合物(括号内为杂质) | 除杂试剂或方法 |
A | CO2(CO) | 点燃 |
B | 铁粉(铜粉) | 加入足量盐酸,过滤 |
C | 氯酸钾(氯化钾) | 加入少量二氧化锰,加热 |
D | 氧化钙(碳酸钙) | 高温煅烧 |
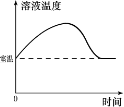
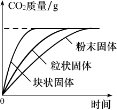
10.下列四个图像中,能正确反映对应变化关系的是 ( )
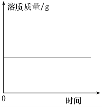
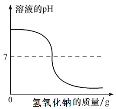
A B C D
A.硝酸铵溶于水时溶液的温度变化 B.等质量碳酸钙与足量同浓度稀盐酸反应
C.将浓硫酸加水稀释成稀硫酸 D.向稀盐酸中不断滴加氢氧化钠溶液
二、选择填充题(本大题包括5小题,每小题3分,共15分。先在A、B、C中选择一个正确选项,将正确选项的代号填在答题卷的相应位置上,然后在D处补充一个符合题意的答案。每小题的选择2分,填充1分)
11.2017年7月,赣州市购置了数台增湿“雾炮车”,有效减少了空气污染,其工作原理是在水喷出前,先将水雾化,以吸收空气中的有害物质。下列物质中属于空气污染物的是 ( )
A.可吸入颗粒物 B.二氧化碳 C.稀有气体 D.
12.下列属于物质化学性质的是 ( )
A.导热性 B.可燃性 C.挥发性 D.
13.2017年冬,我省多个地市爆发流感疾病。专家建议使用磷酸奥司他韦(化学式为C16H28N2O4·H3PO4)等药物进行预防和治疗。下列有关磷酸奥司他韦的说法正确的是 ( )
A.磷酸奥司他韦中含有氮分子
B.磷酸奥司他韦的相对分子质量为410 g
C.1个磷酸奥司他韦分子由58个原子构成
D.磷酸奥司他韦中氮、磷元素的质量比是
14. 如下图所示,用“W”型玻璃管进行微型实验。下列说法正确的是 ( )

A.a处的实验现象为黑色固体粉末变为红色
B.b处的澄清石灰水变浑浊证明有CO2生成
C.a、b两处反应的基本类型分别是置换反应和复分解反应
D.该装置可利用 的方法进行尾气处理
15.如图是a、b、c三种物质的溶解度曲线,下列有关说法正确的是 ( )
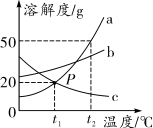 A.P点表示a和c的溶解度均为20 g
A.P点表示a和c的溶解度均为20 g
B.t2℃时,a饱和溶液的溶质质量分数为50%
C.从a和b的混合溶液中提纯a,可采![]() 用降温结晶的方法
用降温结晶的方法
D.将t1℃时a、b、c的饱和溶液升温到t2℃,所得溶液中溶质
的质量分数最大的为
三、填空与说明题(本大题包括5小题,共30分)
16.(3分)将下列短文中带点的部分,用恰当的化学用语填空:
我国古代在认识、改造和应用物质方面有着辉煌的历史。东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”,“曾青”指硫酸铜 溶液;战国《周礼》中记载:“煤饼烧砺房成灰”,“砺房”即牡砺壳,主要成分碳酸钙中碳元素的化合价显+4价 ;蔡伦改进的造纸术,第一步就是将这种“灰”溶于水制得沤浸树皮脱胶的碱液,碱液中含有大量的氢氧根离子 。
17.(7分)走进生活,走进化学
(1)周末小雅妈妈用“加铁酱油”做了“红烧肉”,其中“加铁酱油”中的“铁”是指 (填“元素”或“原子”),炒菜完毕,关闭煤气罐阀门,燃着的煤气熄灭,其灭火的原理是 ; 饭后她用洗洁精清洗了餐具,这是利用了洗洁精的 作用;
(2)家用净水器常用活性炭除去水中的一些杂质,利用了活性炭的 性;
(3)用硬水洗衣服,既浪费肥皂也洗不干净衣服,生活中常用 的方法降低水的硬度。
(4)洗漱时发现卫生间内铁质的置物架生锈了,铁生锈与 有关,为了防止铁制品生锈,可采取的措施是 (填一点)。
18.(6分)甜瓜珍品——江西梨瓜以“脆、甜、香”而闻名。梨瓜中含有丰富的蛋白质、粗纤维、维生素、钙、磷、铁、镁、钾、硒等人体所需的营养素;
(1)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝 防止腐烂;
(2)梨瓜适宜生长在pH为6.0-6.8的土壤中,实验室测定溶液pH的操作方法是 ;
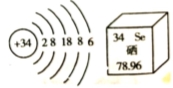
(3)右图为硒元素的某些信息,硒原子核内有 个质子,
硒原子的相对原子质量是 ,硒原子在化学反应中
易 (填“得到”或“失去”)电子。
19.(6分)硅酸钠(Na2SiO3)是我国优先发展的精细化学产品。用某种石英砂矿石(主要成分是SiO2,还含有少量的CuO、Na2SO4、Na2CO3)。工业上制备硅酸钠晶体的流程如下:查阅资料:SiO2既不溶于水,也不与盐酸反应;Na2SO4、Na2CO3均易溶于水。请问答:
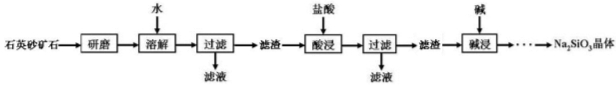
(1)“研磨”的目的是 ;
(2)实验室的过滤操作中必须用到的玻璃仪器有:烧杯、漏斗、 ,过滤时发现过滤速率缓慢,可能原因是 ;
(3)“酸浸”过程中发生反应的化学方程式为 ;
(4)“碱浸”时加入的碱液应选用 (填化学式)溶液。
20.(8分)A~F是初中化学常见的物质,它们均含有同一种元素,其中B与E是植物光合作用的原料,E与F的组成元素相同,D可以用于改良酸性土壤。它们之间的转化关系如图所示![]() (图中“→”表示物质间的转化关系,“—”表示两物质间能发生反应),请回答下列问题。
(图中“→”表示物质间的转化关系,“—”表示两物质间能发生反应),请回答下列问题。
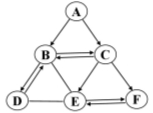
(1)物质F的化学式是_________;
(2)物质E的一种用途为 ;
(3)A→C反应的化学方程式是 ;
(4)B→D的基本反应类型为 。
四、实验与探究题(本大题包括3小题,共25分)
21.![]() (9分)实验室常用块状大理石和稀盐酸反应制取CO2气体。某大理石中因含少量硫化物,使
(9分)实验室常用块状大理石和稀盐酸反应制取CO2气体。某大理石中因含少量硫化物,使
制得的CO2中混有H2S气体。某化学兴趣小组的同学欲用下图装置制取一瓶纯净、干燥的CO2,
请回答下列问题:
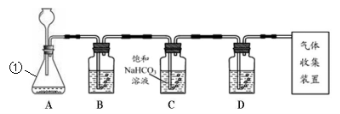
(1)仪器①的名称是 ;
(2)写出实验室制取二氧化碳的化学方程式 ;找出装置A~D中的一处错误并加以改正: ,利用改正后的装置完成后面的实验;
(3)实验室制取的CO2中往往混有少量的HCl气体,其可能原因是 ;混有的HCl气体可用饱和NaHCO3溶液吸收。
(4)小组同学查阅资料得知:H2S能与氢氧化钠溶液、硫酸铜溶液反应。欲除去CO2中混有H2S气体,B装置中所盛试剂应选用 (填“氢氧化钠”或“硫酸铜”)溶液,D装置的作用是 ;
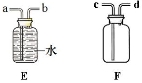
(5)用多功能瓶收集CO2的装置应选用 (填“E”或“F”),气体应从 (填“a”、“b”、“c”或“d”)端导管口通入。
22.(8分)某兴趣小组的同学为探究X、Y、Z三种金属的活动性顺序,设计并完成了下列实验:
实验一:分别把X、Y、Z三种金属放入稀硫酸中,X表面无明显变化,Y表面无明显变化,Z溶解且表面有无色气体产生,溶液最终为无色。请回答:
(1)通过上述实验,你认为上述三种金属中最活泼是 ;
(2) Z与硫酸反应后,生成物中Z显+3价,写出Z与硫酸反应的化学方程式(该金属的化学式用Z表示): ;
实验二:把X、Y分别放入硝酸银溶液中,X表面有银白色固体析出,Y表面没有明显现象。
(3)通过上述实验事实得出X、Y、Z金属活动性由强到弱的顺序为 ;
实验三:小组同学继续对“Z和硫酸反应速率的快慢与什么因素有关”的问题进行探究。下表是他
们分别用质量、形状相同的Z和足量稀硫酸反应的三组实验数据:
实验编号 | 硫酸的质量分数/% | 反应的温度[:] | Z消失的时间/S |
① | 3 | 20 | 500 |
② | 6 | 20 | 300 |
③ | 6 | 30 | 80 |
(4)由实验可知Z和硫酸反应速率与温度的关系是 ;
(5)能证明硫酸的浓度与反应速率关系的实验编号是: ;
(6)该实验除了用Z消失的时间来衡量反应速率的快慢外,请你提出另一种能准确衡量反应快慢的方法或依据: 。
 23.(8分)小明家的下水管道堵塞了,他从超市购买了一种名为“管道通”的药剂,打开包装后发现里面有灰色粉末和白色粉末各一袋,商品的部分标签如图1所示:
23.(8分)小明家的下水管道堵塞了,他从超市购买了一种名为“管道通”的药剂,打开包装后发现里面有灰色粉末和白色粉末各一袋,商品的部分标签如图1所示:
为了弄清这种“管道通”的化学成分和工作原理,小明进行了如下实验探究:
实验一:鉴别A、B粉末的成分,请你将下表补充完整。
实验操作 | 实验现象 | 实验结论 |
取少量灰色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 灰色粉末不溶解, 无明显现象 | 灰色粉末是铝粉[:] |
取少量白色粉末于试管中,加入适量水, 振荡,用手触摸试管外壁 | 白色粉末溶解, | 白色粉末是氢氧化钠 |
实验二:探究管道疏通的原理
【查阅资料】(1)下水管道里的淤积物主要为油污、食物残渣、毛发等;
(![]() 2)氢氧化钠是强碱,能去除油污、腐蚀毛发一类的东西,常用于疏通管道;
2)氢氧化钠是强碱,能去除油污、腐蚀毛发一类的东西,常用于疏通管道;
(3)铝能与氢氧![]() 化钠溶液反应生成偏铝酸钠(NaAl
化钠溶液反应生成偏铝酸钠(NaAl![]() O2)和氢气,同时放出大量的热。偏铝酸钠(NaAlO2)是一种盐,易溶于水,溶液显碱性。写出铝与氢氧化钠溶液反应的化学方程式: 。
O2)和氢气,同时放出大量的热。偏铝酸钠(NaAlO2)是一种盐,易溶于水,溶液显碱性。写出铝与氢氧化钠溶液反应的化学方程式: 。
【进行实验】小明用如图2示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明依次加入铝粉、氢氧化钠和水,并用胶塞堵住弯管上口,观察到的现象
是 ![]() ,堵塞物体变软,落入废液杯中。
,堵塞物体变软,落入废液杯中。
【交流拓展】为了确认实验二中的废液里否有氢氧化钠剩余,小明取少量废液于试管中,滴加几滴酚酞溶液,溶液变红,于是他得出结论:废液中有氢氧化钠剩余。你认为该结论 (填“正确”或“不正确”),理由是 。
五、计算题(本大题包括1![]() 小题,共10分)
小题,共10分)
24.某兴趣小组为探究CaCl2和HCl的混合溶液中CaCl2的质量分数,分别取40g混合溶液,依次加入一定量的Na2CO3溶液,观察到实验中既有气体又有沉淀生成,其中生成沉淀的化学方程式为:
Na2CO3+CaCl2![]() CaCO3↓+2NaCl;充分反应后,过滤、洗涤、干燥并称量,加入的Na2CO3溶液质量与所得沉淀质量关系如下表:
CaCO3↓+2NaCl;充分反应后,过滤、洗涤、干燥并称量,加入的Na2CO3溶液质量与所得沉淀质量关系如下表:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | m | 0 | 1 | 2 | 3 |
| 4 |
(1)上表中m的值为 ;
(2)计算原混合溶液中CaCl2的质量分数;
(3)第⑦次实验后所得溶液中的溶质是 ![]() 。
。
![]()
2018年赣州市初三化学联考试题参考答案
一、单项选择题(每小题2分,共20分)
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
D | A | B[:] | C | C | B | D | A | D | C |
二、选择填充题(本大题包括5小题,每小题3分,共15分)
11. A 一氧化碳、二氧化硫、二氧化氮、臭氧等
12.B 氧化性、还原性、酸碱性、稳定性、金属活动性等
13.C 28︰31
14.B 点燃(或绑一个小气球)
15.C b
三、填空与说明题(本大题包括5小题,共30分)
16.(3分) CuSO4 ![]() OH-
OH-
17.(7分)(1)元素 清除可燃物(或隔离可燃物) 乳化 (2)吸附 (3)煮沸
(4)水和氧气 刷油漆或制成不锈钢等
18.(6分)(1)氧气 (2)用玻璃棒蘸取待测液,滴到pH试纸上,把试纸显示的颜色与
标准比色卡比较,读出溶液的pH (2分) (3)34 78.96 ![]() 得到
得到
19.(6分)(1)加速溶解(或加大反应物之间的接触面积或加快反应速率)
(2)玻璃棒 滤纸没有紧贴漏斗内壁
(3)CuO+2HCl![]() CuCl2+H2O (2分) (3)NaOH
CuCl2+H2O (2分) (3)NaOH
20.(8分)(1)CO(2分) (2)灭火、制作碳酸饮料、光合作用原料等(2分)
(3) 2H2O2 2H2O+O2↑(2分)(4)化合反应(2分)
四、实验与探究题(本大题包括3小题,共25分)
21.(9分)(1)锥形瓶;(2)CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;(2分)
长颈漏斗未液封,长颈漏斗下端应伸入到液面下(3)盐酸浓度较高或盐酸有挥发性;
(4)硫酸铜 除去水蒸气; (5)F c
22.(8分)(1)Z;(2)2Z+3H2SO4==Z2(SO4)3+3H2↑(2分)(3)Z>X>Y
(4)温度越高,反应速率越快(5)①②(6)相同时间内产生气体的体积(2分)
23.(8分)实验一:试管外壁发烫
实验二:【查阅资料】(3)2Al+2NaOH+2H2O ![]() 2NaAlO2+3H2↑(2分)
2NaAlO2+3H2↑(2分)
【进行实验】弯管外壁发烫(或弯管内的温度明显升高)、产生大量气泡(2分)
【交流拓展】不正确 偏铝酸钠溶液显碱性,也能使酚酞溶液变红(2分)
五、计算题(本大题包括1小题,共10分)
24.(1)_0 (2分)
(2)解:设原混合溶液中CaCl2的质量为x (0.5分)
Na2CO3+CaCl2![]() CaCO3↓+2NaCl
CaCO3↓+2NaCl
![]() 111 100 (1分)
111 100 (1分)
x 4g (1分)
111/100﹦x/4g (1分)
x﹦4.44g (1分)
CaCl2的质量分数为![]() :4.44g/40g×100%﹦11.1%(1分)
:4.44g/40g×100%﹦11.1%(1分)
答:原混合溶液中CaCl2的质量分数11.1%。(0.5分)
(3)Na2CO3、NaCl (2分)

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...