2018年四川省达州中学九年级化学模拟测试题【word版】
为了方便您的阅读请点击全屏查看
11、日常生活中,我们经常饮用矿泉水.右图是某饮用天然水检测结果.去年上半年,我省部分市区持续严重干旱,造成人、畜饮水困难.水是生命之源,应该爱护水资源.下列净化水的方法中发生了化学反应的是( )
A. 通过蒸馏来净化水 B. 通过消毒来净化水
C. 用活性炭来净化水 D. 用明矾来净化水
12、中国诗词既蕴含人文思想,又焕发理性光辉.对下列划线部分的化学解释不合理的是( )
A. 花气袭人知骤暖,喜鹊穿树喜新晴−温度高分子运动加快
B. 何意百炼钢,化为绕指柔−生铁经不断煅烧捶打氧化,降低碳的含量,变成钢
C. 千锤万凿出深山,烈火焚烧若等闲−煅烧石灰石,不发生化学变化
D. 美人首饰侯王印,尽是沙中浪底来−金的性质稳定,在自然界中以单质形态存在
A. ![]()
B. ![]()
C. ![]()
D. ![]()
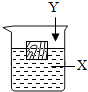 14、如图,一木块漂浮于X中,向X中缓缓加入(或通入)少量物质Y后最终木块上浮,则X与Y可能是(溶液的体积变化忽略不计)( )
14、如图,一木块漂浮于X中,向X中缓缓加入(或通入)少量物质Y后最终木块上浮,则X与Y可能是(溶液的体积变化忽略不计)( )
序号 | X | Y |
① | 水 | 食盐 |
② | 氢氧化钙溶液 | 二氧化碳 |
③ | 稀硫酸 | 镁粉 |
④ | 硫酸铜溶液 | 铁粉 |
A. ②④ B. ①③ C. ①②③ D. ②③④
15、除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
序号 | 物质 | 杂质 | 试剂 | 操作 |
A | Cu(NO3)2溶液 | AgNO3溶液 | Cu | 过滤 |
B | Na2CO3 | NaHCO3 | 盐酸 | 结晶 |
C | Fe | Cu | 稀硫酸 | 过滤 |
D | CO2[:] | HCl | N | 洗气 |
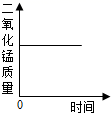

A、硫在含有氧气的密闭容器内燃烧, B、往二氧化锰中加入过氧化氢溶液[:学,科,网]
 容器内原子个数随时间变化的关系 ,二氧化锰质量随时间变化的关系
容器内原子个数随时间变化的关系 ,二氧化锰质量随时间变化的关系
.
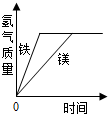
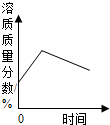
C、等质量的镁粉和铁粉分别与过量且浓 D. 在恒温条件下往饱和蔗糖溶液
度相同的稀盐酸反应,放出的氢气质 中不断加入蔗糖固体,溶质质量
量随时间变化的关系 分数随时间变化的关系
17、利用下列各组物![]() 质不能验证Fe、Cu、Ag三种金属活动性顺序的是( )
质不能验证Fe、Cu、Ag三种金属活动性顺序的是( )
A. Cu、AgNO3溶液、FeCl2溶液 B. Fe、Cu、Ag、稀盐酸
C. Fe、Ag、CuSO4溶液 D. Fe、Cu、稀硫酸、AgNO3溶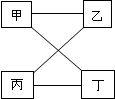 液
液
下表提供的四组物质,符合图示相连物质间在一定条件下可以发生反应的是( )
| 甲 | 乙 | 丙 | 丁 |
A | Mg | HCl | CuSO4 | N |
B | CO | O2 | H2SO4 | CuO |
C | KOH | SO3 | NaOH | CuSO4 |
D | Na2CO3 | Ca(OH)2[:.Com] | HCl | CaCl2 |
二、填空题(本大题共5小题,共25分)
44、(5分)用化学符号和数字表示:
(1)两个铁离子 ______ ;(2)硝酸银中银元素的化合价 ______ ;
(3)铝制品在空气中表面失去金属光泽所形成的物质 ______
(4)构成氯化钠的微粒: ______ ;
(5)海水中含量最多的金属元素与非金属元素组成的化合物: ___ ![]() ___ ;
___ ;
46、(4分)如表是元素周期表中第2、3周期的元素,请回答有关问题.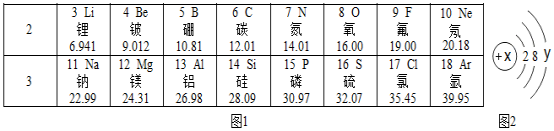
(1)下列各组具有相似化学![]() 性质的元素是______(填字母序号);
性质的元素是______(填字母序号);
A.Na、Cl B.O、S ![]()
C.F、Cl D.Cl、Ar
(2)写出一条第三周期元素原子的核外电子排布规律______;
(3)第7号元素与第12号元素的原子形成化合物的化学式为______;
(4)某离子的结构示意图如图2所示,当x−y=8时,该粒子的符号为______;
47、(7分)结合水和溶液的相关知识,回答下列问题:
(1)对![]() 于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是 ______ .
于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是 ______ .
(2)水是化学实验中常用的试剂,下列各组物质能用水鉴别的是 ______ (填字母).
A.氢氧化钠和硝酸铵 B.食盐和蔗糖 C.高锰酸钾和氯酸钾
(3)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是 ______ .
①溶解 ②把配好的溶液装入细口瓶 ③称量 ④计算 ⑤量取 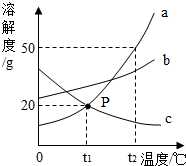
(4)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
①P点的含义是 ___ .
②在t2℃时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是 ______ 克.
③将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,所得溶液中溶质质量分数大小关系是 ___ ___ .
④a物质中含有少量c物质,可用 ______ 方法提纯a物质(填“降温结晶”或“蒸发结晶![]() ”).
”).
三、探究题(本大题共2小题,共20.0分)
(4)如图F所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是______。
(5)图G和图B都可用作实验室用锌粒和稀硫酸反应制取氢气的发生装置,G装置与B装置比较,所具有的操作上的优点是______。
(6)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(化学式:NH3),常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。制取并收集NH3,应该从图中选择的发生装置是______ (填序号),收集装置是______ (填序号)。
(1)白色沉淀A是CaCO3,请写出生成该沉淀的化学方程式___ .
(2)滤液B中含有Na2CO3、NaOH、NaCl三种溶质.
【实验验证】为证明滤液B中存在的三种溶质,同学们进行了如下实验.
步骤 | 实验操作 | 实验现象 |
|
I | 取少量滤液B于试管中,加入过量 的Ba(NO3)2溶液,过滤 | ______ |
|
II | 取少量步骤 I中所得滤液 加入酚酞溶液 | ______ | |
III | 另取少量步骤 I中所得滤液于试管中,先加入足量的稀硫酸,再加入 ______ 溶液 | 产生白色沉淀 |
【拓展提升】
①向步骤I中加入过量Ba(NO3)2溶液的目的是______.
②小妮同学认![]() 为若将步骤I中的Ba(NO3)
为若将步骤I中的Ba(NO3)![]() 2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质.你认为是否合理______(填“合理”或“不合理”).
2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质.你认为是否合理______(填“合理”或“不合理”).
③小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由______.
四、计算题(本大题共1小题,共6.0分)
51、徐州地区石灰石资源丰富.某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10g | 3.0g |
第二次加入10g | 2.0g |
第三次加入10g | l.0g |
笫四次加入10g | 0.6g |
请计算:
(1)4.0g石灰石样品中碳酸钙的质量是 ______ g.
(2)10g稀盐酸能与 ______ g碳酸钙正好完全反应.
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1% ).

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...