2018年石家庄中考化学压轴试题【可下载含答案】
由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看!
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5
一、选择题(共 20 个小题,每小题 2 分,满分 40 分,在每小题的 4 个选项中只有一个符合题意。)
1.下列各组物质混合搅拌后,能形成溶液的是
A.面粉和水 B.汽油和水 C.蔗糖和水 D.食用油和洗涤剂
2.下列关于溶液的叙述,正确的是
A.无色透明的液体一定是溶液 B.溶液中各部分的性质均相同
C.饱和溶液不能再溶解任何物质 D.溶液中只能有一种溶质
3.根据你所做过的家庭小实验,判断下列液体能导电的是
A.稀硫酸 B.酒精溶液 C.蔗糖溶液 D.蒸馏水
4.下列实验操作中,不正确的是
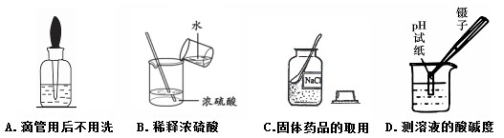
5.下列选项中物质的名称,俗名,化学式不一致的是
A.氧化钙 生石灰 CaO B.碳酸钠 纯碱 Na2CO3
C.银 水银 Ag D.氢氧化钠 苛性钠 NaOH
6.我们已经熟悉的下列物质中,溶于水或与水反应时不会放出大量热量的是
A.生石灰 B.NaOH 固体 C.浓硫酸 D.食盐
7.下列关于盐酸、硫酸的说法错误的是
A.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
B.用浓盐酸吸收氧气中的水蒸气
C.浓硫酸露置于空气中,溶质的质量分数会变小
D.浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上 3%~5%的碳酸氢钠溶液
8.下列反应中属于中和反应的是
A.CaCO3+2HCl== CaCl2+H2O+CO2↑ B.CuO+H2SO4== CuSO4+H2O
C.SO3+2NaOH==Na2SO4+H2O D.Cu(OH)2+2HCl==CuCl2+2H2O
9.如图两圆相交部分是五种物质中两两之间相互反应的
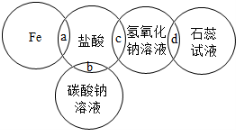 示意图。下列对反应现象的说法中,错误的是
示意图。下列对反应现象的说法中,错误的是
A.a 处形成浅绿色溶液 B.b 处形成大量气泡 C.c 处反应放热
D.d 处溶液呈红色
10.从海水中提取食盐的流程如下,下列说法错误的是
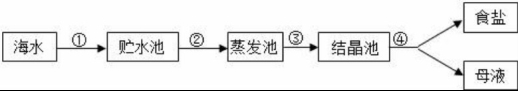
A.经过第①步操作,海水中的成分基本不变 B.蒸发池中,氯化钠溶液逐渐变浓 C.经过第③步的操作,进入结晶池后,继续蒸发水,有④发生 D.析出食盐晶体后的母液是氯化钠的不饱和溶液
11.对物质进行分类是化学学习中重要的环节,下列物质分类错误的一组是
A.单质:H2、O2、N2 B.酸:HCl、H2SO4、CuSO4
C.碱:NaOH、Ba(OH)2、NH3•H2O D.盐:NaNO2、CaCO3、KMnO4
12.许多同学喜欢用“雪碧”之类的碳酸饮料,下列有关“雪碧”的叙述正确的是 A.饮用“雪碧”会使人体血液的 pH 升高
B.喝“雪碧”会打嗝.是因为“雪碧”受热,溶解在其中的 CO2 的溶解度变小 C.往“雪碧”中滴加酚酞试液,无色酚酞试液变红色 D.胃酸过多的病人可以多喝碳酸饮料
13.下列实验数据合理的是
A.用 pH 试纸测得某地雨水的 pH 为 5.6
B.用 10 mL 量筒量取了 6.53 mL 水
C.用 20 g 氯化钠和 100 g 水配制的 120 g 食盐水,其溶质质量分数为 20%
D.用托盘天平称得某纯碱样品的质量为 10.2g
![]()
![]()
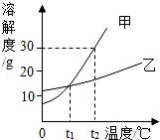 14.甲、乙两种固体物质的溶解度曲线如图所示。下列叙述中正确的
14.甲、乙两种固体物质的溶解度曲线如图所示。下列叙述中正确的
是
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两物质饱和溶液的溶质质量分数一定相等
C.t2℃时,将 30g 甲物质放入 70g 水中,所得饱和溶液的质量为100g
D.t2℃时,甲、乙两物质的饱和溶液降温到 t1℃,析出晶体质量甲>乙
15.推理是化学学习中常用的思维方法。下列推理正确的是 A.酸溶液中都含有 H+,所以酸溶液有相似的化学性质 B.铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 C.碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的一定是碱溶液 D.复分解反应的反应物、生成物都是两种化合物,则反应物和生成物都是两种化合物的反应
一定属于复分解反应
16.下列各组常见的固体物质中,用水不能区分的是
A.NaOH 和 NH4NO3 B.CuSO4 和 Na2SO4
C.Na2CO3 和 CaCO3 D.NaCl 和 KCl
17.在一定条件下,下列转化不能一步实现的是
A.H2O→H2 B.Ca(OH)2→NaOH C.CuO→CuCl2 D.Fe→Fe2(SO4)3
18.除去下列物质中含有的少量杂质(括号内的物质),所选试剂不合理的是 A.CaO(CaCO3):稀盐酸 B.NaOH 溶液[Ca(OH)2 溶液]:碳酸钠溶液 C.Cu(Fe):硫酸铜溶液 D.CO(CO2):氢氧化钠溶液
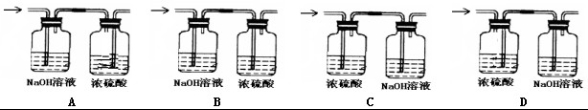 19.为除去氢气中含有的少量氯化氢气体和水蒸气,应选用的装置是图中的
19.为除去氢气中含有的少量氯化氢气体和水蒸气,应选用的装置是图中的
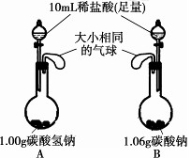
20.某同学用右图所示装置进行实验。将等浓度、等体积的足量稀盐酸同时加入到分别盛有碳酸
![]() 氢钠和碳酸钠的烧瓶(大小相 同)中。可以观察到的现象:①两只烧瓶中都有气泡冒出;②两只烧
氢钠和碳酸钠的烧瓶(大小相 同)中。可以观察到的现象:①两只烧瓶中都有气泡冒出;②两只烧
瓶中的固体最终全部溶解;③最终气球鼓起程度 A 大于 B;④最终气球鼓起程度 B 大于 A;⑤最终
 气球鼓起的程度 A 和 B 相同。其中正确的是
气球鼓起的程度 A 和 B 相同。其中正确的是
A.①④ B.①②④
C.①②⑤ D.①②③
二、填空及简答题(共 6 小题,除 21 题外每空 1 分,满分 41 分)
21.(每空 2 分)写出生活中下列物质或其主要成分的化学式:
①烹饪时做调味品的是 ;②洁厕灵中含有的酸 ;③炉具清洁剂中含有的
碱 ;④小苏打 ;⑤汽车用铅蓄电池中含有的酸 ;⑥可用作
建筑材料的盐是 ;⑦侯氏制碱法中“碱”指的是 。
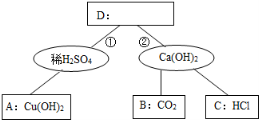 22.如图为酸碱的化学性质知识网络,A、B、C、D
22.如图为酸碱的化学性质知识网络,A、B、C、D
是四种常见不同类别的化合物,图中短线表示两种 物质在一定条件下可以发生化学反应,请你据图回 答:(1)A、B、C 三种物质中,不能用来鉴别稀硫酸 与氢氧化钙溶液物质是 ;
(2)D 物质可以是 (填“碳酸钾”、“碳酸钙”、“硝酸钡”或“氯化钠”),反应①实验现 象 。
23.按要求书写下列各反应的化学方程式:
(1)某食品包装袋中干燥剂的主要成分是生石灰,其能干燥食品的原因 ;
(2)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是 CaCO3 和 Mg(OH)2],可以用稀盐酸来
洗涤,写出与 Mg(OH)2 反应的化学方程式 ;
(3)氯化钡溶液与硫酸铜溶液反应 ;
(4)AgNO3 溶液与 Cu 反应 。
![]()
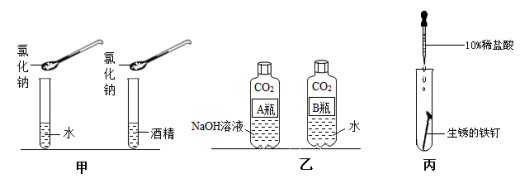 24. 根据下列三个实验,回答问题:
24. 根据下列三个实验,回答问题:
(1)实验甲是探究 NaCl 在不同溶剂中的溶解性,应该保持相同的物理量是 (填字母序号)。
A.温度 B.NaCl 的质量 C.水和酒精的质量
(2)实验乙:将等体积的氢氧化钠溶液、水分别倒入集满二氧化碳的质地较软的塑料瓶中,拧紧瓶
盖,充分振荡,观察到 ,证明 。 写出该实验中发生反应的化学方程式 (任写一个)。
(3)实验丙:刚开始滴加稀盐酸时的实验现象是 ,写
出发生反应的化学方程式 。继续滴加稀盐 酸浸没钉子,过一段时间,又会发现有 产生, 写出发生反应的化学方程 式 。实验能体现出稀盐酸具有的化学性质是
、 。
25.某化学兴趣小组三位同学在学习盐酸与氢氧化钠反应后,分别结合自己在实验室中所做的实 验,各从不同方面对其进行图象描述:图 A 是实际操作图,图 B 是反应过程中溶液的酸碱度变化 图,图 C 是微观粒子结合过程的示意图。
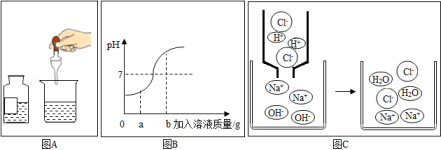
根据图 B 的曲线变化,回答下列问题:
(1)该变化对应的实验操作是将 滴加到另一种溶液中。
(2)当滴入溶液的质量为 a g 时,溶液中的溶质为 (填化学式)。
(3)当溶液的 pH=7 时,溶液中的主要离子是 (填离子符号)。
(4)当加入溶液的质量为 b g 时,向所得溶液中滴加紫色石蕊试液,溶液是 色。
(5)关于实验中的细节分析:
①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是 ;
②实验过程中,要用玻璃棒不断搅拌,这样做的目的是 。
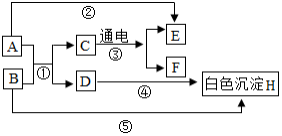 26. A﹣H 是初中化学常见的物质,其相互转
26. A﹣H 是初中化学常见的物质,其相互转
化关系如图所示,其中 A 是人体胃液中帮助消
化的物质,B 用于改良酸性土壤。
(1)D 的化学式为 。
( 2 ) 写 出 反 应 ② 的 化 学 方 程
式 。
(3)指出反应①的基本反应类型 。
(4)指出物质 H 的一种用途 。 三、实验探究题(共 2 个小题,每空 1 分,共 13 分)
27.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制 50 g 5%的
氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。
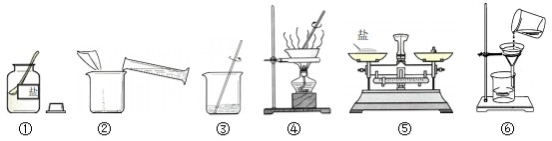
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 。
(3)粗盐提纯实验的操作顺序为(填操作序号) 、 称量精盐并计算产率。
(4)操作④中,当观察到 时,停止加热。
实验二:用提纯得到的精盐配制了 50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因
可能有 (填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
![]()
28.某同学发现,上个月做实验用的 NaOH 溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开 始实验探究。
【猜想假设】猜想 1:该溶液没有变质,为 NaOH 溶液。 猜想 2:该溶液全部变质,为 Na2CO3 溶液。
猜想 3:该溶液部分变质,为 。
 【设计方案】请你完善下表几组同学探讨的设计方案:
【设计方案】请你完善下表几组同学探讨的设计方案:
四、计算题(共 1 个小题,第 1 问 1 分,第 2 问 5 分,共 6 分)
29.某石油化工厂化验室的实验员用 15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测
 得实验数据如下表:
得实验数据如下表:
![]()
| 实验操作 | 可能出现的现象与结论 | 同学评价 |
第 1 组 |
|
若溶液变红,则猜想 2 不成立 |
第 2 组同学认为:此方 案结论不正确,理由是 |
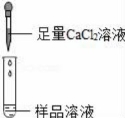
第 2 组 |
|
若 ,反 应 方 程 式: , 则猜想 1 不成立 |
第 3 组同学认为:此方 案还不能确定猜想 2 还 是猜想 3 成立 |
第 3 组 | 第一步 第二步 |
若 滤 液 不 变 红 ,则 猜 想 2 成 立;若滤液变红,则猜想 3 成 立 |
第 1 组同学认为:不需 过 滤 也 能 达 到 实 验 目 的,更简单的操作方法 是: |
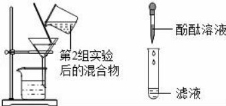 【探究实验】综合各小组的方案后,动手实验。
【探究实验】综合各小组的方案后,动手实验。
【结论】NaOH 溶液易与空气中 CO2 反应而变质,所以 NaOH 溶液要 保存。
【反思】实验结束后,还有同学认为,第 2 组同学的 CaCl2 溶液可换成 Ca(OH)2 溶液,同样也能完 成本实验,你是否赞成 (填“是”或“否”)理由是 。
请回答下列问题:
(1)欲计算出一定量石油产品中所含 H2SO4 的质量,你觉得应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为 100g,请计算该残余硫酸的溶质质量分数。
![]()
2018年石家庄中考化学压轴试题参考答案
一、选择题 (每小题 2 分,共 40 分)
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C | B | A | C | C | D | B | D | D | D |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
B | B | D | B | A | D | D | A | B | D |
二、(21 题每空 2 分,其余每空 1 分,共 41 分)
21.NaCl HCl NaOH NaHCO3 H2SO4 CaCO3 Na2CO3
22.(1)CaO+H2O=Ca(OH)2 (2)Mg(OH)2+2HCl=MgCl2+2H2O (3)BaCl2 + CuSO4 = BaSO4
↓ + CuCl2 (4)2AgNO3+Cu=2Ag+Cu(NO3)2
23.(1)C 或 HCl (2)碳酸钾 有气泡产生
24.(1)ABC (2)A 瓶比 B 瓶更瘪 NaOH 能与 CO2 反应 CO2+H2O=H2CO3 或 2NaOH+CO2
=Na2CO3+H2O
(3)铁锈逐渐消失,溶液变成黄色 Fe2O3+6HCl=2FeCl3+3H2O 气泡 Fe+2HCl=FeCl2+
H2↑ 能与金属氧化物(Fe2O3)反应 能与活泼金属(Fe)反应
25.(1)NaOH 溶液 (2)NaCl、HCl (3)Na+、Cl— (4)蓝 (5)防止盐酸过量 使加入的氢
氧化钠与盐酸充分反应
26.(1)CaCl2 (2)Mg+2HCl=MgCl2+H2↑ (金属也可用 Zn、Fe、Al)(3)复分解反应 (4) 作建筑材料或补钙剂
三、(每空 1 分,共 13 分)
27.加速食盐的溶解 没有用玻璃棒引流 ①⑤②③⑥④ 出现较多固体 ①②③
28.【猜想 3】NaOH 和 Na2CO3 的混合溶液
【设计方案】第 1 组评价:Na2CO3 溶液显碱性,也能
使酚酞溶液变红 第 2 组现象与结论:有白色沉淀产生 CaCl2 +Na2CO3 =CaCO3↓ +2NaCl
第 3 组评价:将第二组实验沉淀之后取滤液(表达合理即可)
【结论】密封
【反思】否
Ca(OH)2与 Na2CO3 反应会生成 NaOH,就不能确认原溶液中是否再含 NaOH
四、(1 分+5 分=6 分)
29.(1)②
(2)7.35%
![]()

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...