![]() 2018重庆市中考化学模拟试题【精编Word版含答案】
2018重庆市中考化学模拟试题【精编Word版含答案】
注意:由于格式问题,部分试题考生在预览时会出现乱码情况,如有此现象发生,请点击全屏查看。
(总分70分 物理和化学共120分钟完卷)
可能用到的相对原子质量:H—1 O—16 Ca—40 P—31
一.单项选择题(本大题包括16个小题,每小题2分,共32分)
1. 下列农副产品在加工过程中,主要发生化学变化的是…………………………( )
A.楠竹加工成凉席 B.鲜鸭蛋制成松花皮蛋
C.茶叶压制成茶饼 D.油菜籽压榨出菜油
2. 请各位答题的同学深呼吸平静一下情绪,刚才吸入的空气中含量最多的气体是( )
A.氧气 B.稀有气体 C.氮气 D.二氧化碳
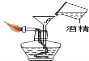
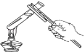
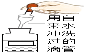
3. 下列图示中的“错误实验操作”与图下面对应的“可能产生的后果”不一致的是…( )
A.液体喷出 B.污染试剂 C.酒精溅出 D.读数偏大
4.对下列宏观事实的微观解释,不合理的是………………………………………( )
A.氧化汞受热后分解---分子在化学变化中可分 B.车胎在阳光下爆裂----分子体积变大
C.闻到不远处的花香------分子在不断地运动
D.1滴水中大约有1.67×1021个水分子------分子的质量和体积小
5. 2017年“中国水周”活动的宣传主题是“落实五大发展理念,推进最严格水资源管理”.下列做法不符合这一主题的是…………………………………………………… ( )
A.逐步淘汰高耗水生产工艺 B.农作物采用大水漫灌
C.生活污水集中处理后排放 D.大量开采和使用地下水
6.对下列四种粒子的结构示意图的理解,错误的是………………………………( )
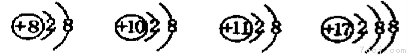
A.它们属于不同种元素 B.它们都具有相对稳定结构
C.它们的核外电子排布不完全相同 D.它们都带电荷
7.鉴别空气、氧气和二氧化碳三瓶气体,最常用的方法是…………………………( )
A.分别测定它们的密度 B.将燃着的木条分别伸入集气瓶中
C.观察颜色并闻它们的气味 D.将气体分别通入澄清石灰水中
8.下列说法不正确的是…………………………………………………………………( )
A.在NO2中不含氧分子 B.钠离子得电子变成钠原子
C. 镁离子的符号是Mg2+ D.氧气中氧元素的化合价为-2价
9.葡萄糖的化学式为C6H12O6,下列有关葡萄糖的说法正确的是…………………………( )
A.葡萄糖由24个原子构成 B.葡萄糖分子由碳原子和水分子构成
C.葡萄糖由碳、氢、氧三种物质组成 D.葡萄糖由三种元素组成
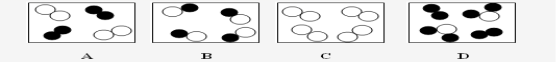
10.用“![]() ”和“
”和“![]() ”表示不同元素的原子,下列微观示意图既有单质又有化合物的是
”表示不同元素的原子,下列微观示意图既有单质又有化合物的是
……………………………………………………………………………………… ( )
11.科学家发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。据此推断,
当一种元素的原子经过放射变化后,结果变成了另一种元素的原子。它一定是放射了( )
A.电子 B.中子 C.质子 D.该原子的原子核
12.右图为小明制作的原子模型,下列说法正确的是…………………………………… ( )
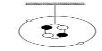
A.该模型表示一种碳原子 B.该原子的核电荷数为4
C.该原子的质量主要集中在2个电子上
D.该原子核由2个质子和2个中子构成
13.NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时不能生成的物质是( )
A.CO2 B.Cl2 C.O2 D.N2
14.蜡烛(足量)在如右图密闭装置内燃烧至熄灭,用仪器测出这一过程中
瓶内氧气含量的变化如右图所示。下列判断正确的是…………………………………( )
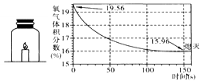
A.蜡烛燃烧属于化合反应
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.蜡烛熄灭后瓶内只剩二氧化碳气体
D.该方法可用于测定空气中氧气的体积分数
15.某高性能锂电池其反应原理可表示为:Li+MnO2=LiMnO2 , 已知锂元素在化合物中显+1价,下列说法正确的是……………………………………………………………………( )
A. LiMnO2是氧化物 B.该反应是化合反应
C.此反应中,二氧化锰是催化剂 D.LiMnO2中锰元素的化合价显+2价
16. 下列图象不能正确反映对应变化关系的是( )
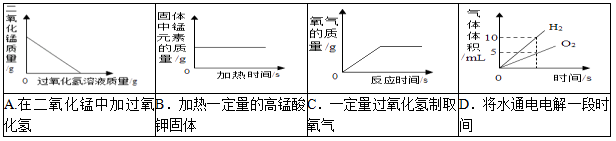
二.填空题(本大题包括5个小题,每空1分共20分)
17.请按要求填空。
(1) 氖气______ 2个氮分子______ 1个硝酸根离子_____
3个汞原子 地壳中含量最多的金属元素是_________(填名称)
⑵已知亚硫酸的化学式是H2SO3 ,试写出亚硫酸钠的化学式________
(3) 消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为________ 。
18. 近几年来,雾霾在我国多地频发,严重危害了人体健康。大量化石燃料的燃烧是导致这
一现象的主要原因。雾霾可导致呼吸系统疾病病人增多,因为雾霾会使空气中增加大量的 ______ (填字母序号,下同),下列气体大量排放到空气中,会形成酸雨的是 ________ 。
A.一氧化氮 B.一氧化碳 C.二氧化硫 D.可吸入颗粒物.
为防止空气污染,保护蓝色美丽的天空,你有什么好的建议(写一条)
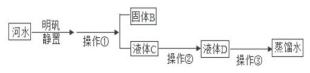
19.小明收集到一瓶浑浊的黄河水,他要模拟自来水厂的净水过程,最终制成蒸馏水,其实验过程如下所示。请回答以下题。
(1)其中明矾的作用是 ___________ ,
操作①的名称是 ___________,在进行操作①时,小明发现所用的时间比较长,其原因可能是 ________
a.漏斗内的滤纸有破损 b.搅拌浑浊后未静置直接倒入漏斗过滤
c.滤纸没有紧贴漏斗内壁 d.漏斗内液面高于滤纸的边缘
(2)操作②是杀菌消毒,属于_________变化,日常生活中硬水转化成软水的方法是___________
![]()
20.分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系
的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
A.水银 B.蒸馏水 C.氯酸钾 D.四氧化三铁
21. 按要求回答下列问题。
(1) 向盛有蒸馏水的试管中加5滴酚酞水溶液,无明显现象,再加入浓氨水,会出现_____ 色;
(2) 按右图所示进行实验探究,用大烧杯罩住A、C两个小烧杯一段时间后,A烧杯中溶液变色。
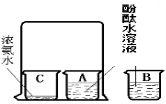 贝贝同学提出了以下几种假设:
贝贝同学提出了以下几种假设:
假设1 空气中的氮气使酚酞溶液变色
假设2 空气中的氧气使酚酞溶液变色
假设3 浓氨水中的氨分子运动使酚酞溶液变色
假设4浓氨水中的水分子运动使酚酞溶液变色
你认为假设 _____不能成立,理由是
(3) 为了验证剩下几种假设的正确性,小马同学增加了烧杯B作对比实验,烧杯B能够否定假设 的合理性。
三.实验题:(本大题包括2个小题,每空1分,共11分)
22. (5分)
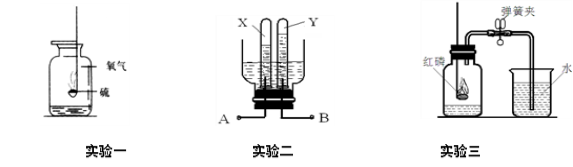
以下是初中化学常见实验,请回答有关问题。
(1) 实验一的集气瓶中预先加入了少量水,其作用是 ;
(2) 实验二为电解水的实验,其中A是与电源的 极相连。通电后,发生反应的
符号(或文字)表达式为 ;
实验刚开始时,X和Y气体的体积比>2:1,则可能原因是 (填序号);
①氧气溶解的更多 ②氢气溶解的更多 ③氧气密度大 ④氢气密度小
⑤氧气与电极发生了反应 ⑥水中未加入少量硫酸钠或氢氧化钠
(3)实验三是测定空气中氧气的含量。假如集气瓶容积为100mL,实验前已经装水
20mL,则实验后集气瓶内的水约是 mL。
23.某学习小组围绕“气体实验室制取”进行了研讨。请你参与完成下面的问题
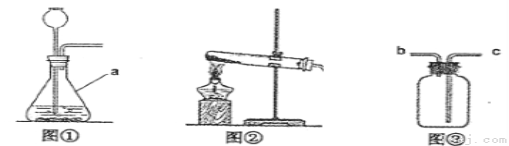
(1)原理分析:实验室用过氧化氢溶液制取O2的符号表达式为 。
(2)发生装置:图①装置中仪器a的名称是 。实验室常用无水醋酸钠固体与碱石灰在加热的情况下制CH4,应选图 作 发生装置。(填序号)
(3)收集装置:已知有毒气体SO2密度大于空气,收集SO2时,常采用图③收集,气体应
从 端通入(填字母)。
(4)实验操作:用KMnO4制取O2的操作过程可概括为“组装仪器→ →装入药品→加热试管→收集气体→停止加热”。
(5)实验反思:在加热KClO3制O2的过程中,发现产生O2的速率很慢,经检查不是KClO3变质,也不是装置气密性不好,你认为最可能的原因是 。
四.计算题(本大题只有1个小题,共7分)
24.人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体〔Ca10(PO4)6(OH)2〕形式存在。牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。下图是某乳业公司纯牛奶包装标签的部分文字。请仔细阅读后回答下列问题:
纯牛奶 配料:鲜牛奶 保质期:8个月 净含量:250 mL/盒 营养成分(每100 mL):钙≥0.11 g 脂肪≥3.3 g 蛋白质≥2.9 g |
(1)羟基磷酸钙〔Ca10(PO4)6(OH)2〕中钙元素、磷元素、氧元素、氫元素的质量比是
(最简整数比)
(2)包装标签上脂肪≥3.3 g,是指100 mL牛奶中含脂肪至少3.3 g。那么一盒牛奶中含钙至少
g。(保留到0.01 g)
(3)求羟基磷酸钙中钙元素的质量分数(保留到0.1%)。(写出计算过程)
(4)若人体每天至少需要0.6 g钙,且这些钙有90%来自牛奶,则一个人每天至少喝多少盒牛奶?(写出计算过程)
2018重庆市中考化学模拟试题答题
一.单项选择题(本大题包括16个小题,每小题2分,共32分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
二.填空题(本大题包括5个小题,每空1分共20分)
17.请按要求填空。
⑴
⑵ ⑶
18.
19. ⑴
⑵
20.
21.⑴
⑵
⑶
三.实验题:(本大题包括2个小题,每空1分,共11分)
22.⑴
⑵
⑶ mL
23.⑴
⑵
⑶ ⑷
⑸
四.计算题(本大题只有1个小题,共7分)
⑴ (最简整数比)
⑵ g (保留到0.01 g)
⑶写出计算过程(保留到0.1%)
⑷写出计算过程(结果保留整数)

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...