由于格式问题此试题可能会出现乱码的情况
为了方便您阅读请点击右上角的全屏查看
2018乐山市中考化学压轴试题
17.下列说法属于化学性质的是


18.右图是某化肥包装袋上的部分说明,该化肥属于
A.氮肥 B.磷肥
C.钾肥 D.复合肥料
19.5月31日是“世界无烟日”,香烟燃烧产生烟尘、尼古丁、焦油、CO等多种有害物质,青少年朋友要远离烟草,养成良好的生活习惯。下列有关说法正确的是
A.香烟装有过滤嘴,所以吸烟对人体无害 B.香烟烟气中只有尼古丁有毒
C.香烟烟气中的CO比O2更容易与血红蛋白结合
D.吸烟只影响自己的健康,不影响他人健康
20.近年来。“雾霾天气”已经严重影响到人们的生活质量和健康水平,下列情况不会加重“雾霾天气”的是
A.用氢气作燃料 B.露天焚烧垃圾 C.汽车排放尾气 D.用煤作燃料
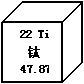 21.钛和钛合金是21世纪的重要材料,具有很多优良性能。钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见下图。下列说法中错误的是
21.钛和钛合金是21世纪的重要材料,具有很多优良性能。钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见下图。下列说法中错误的是
A.钛元素原子的质子数为22
B.钛元素属于非金属元素
C.钛元素的相对原子质量为47.87
D.钛元素与氯元素组成的化合物化学式为TiCl4
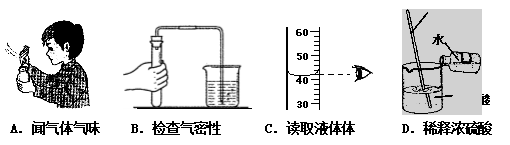 22.(乐山市中考化学)下列实验操作错误的是
22.(乐山市中考化学)下列实验操作错误的是
23.下列各组物质中,带点的同种元素化合价相同的是
A.Cl2、NaCl B.NH4Cl、HNO3 C.MnO2 、K2MnO4 D.P2O5、Ca3(PO4)2
24.“成昆复线”的修建将进一步推动我省经济的发展。在修筑铁路的土石方爆破中要用到黑火药,爆炸时反应为:2KNO3+S+3C![]() K2S+3CO2↑+X↑,其中X的化学式是
K2S+3CO2↑+X↑,其中X的化学式是
A.N2 B.NO2 C.NO D.N2O
25.右图是工业上制备氢气的微观示意图,其中不同的“球”代表不图的原子。下列说法不正确的是

![]() A.图中“ ”表示氢分子
A.图中“ ”表示氢分子
B.反应前后,原子的种类、数目不变
 C.该反应中参加反应的两种分子的个数比为1:1
C.该反应中参加反应的两种分子的个数比为1:1
D.该反应前后共涉及两种单质和两种化合物
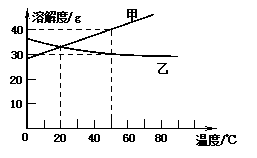
26.右图是甲、乙两种固体物质的溶解度曲线,
下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.乙的不饱和溶液降温可变成饱和溶液
C.20oC时,甲、乙两种物质的溶解度相等
D.50oC时,甲的饱和溶液中溶质的质量分数为40%
27.将金属M置于硫酸锌溶液中,无明显现象发生;而将其置于硫酸铜溶液中,表面有红色固体物质析出。由此可判断M、Zn、Cu的金属活动性由强到弱的顺序为
A.M、Zn、Cu B.Zn、M、Cu C.Zn、Cu、M D.Cu、 M、Zn
28.下面是某同学整理的部分化学知识,其中有错误的是
A.地壳中几种元素含量的比较:O>Si>Al
B.构成物质的几种粒子:分子、原子、离子
C.常见的碱:NaOH、KOH、Ca(OH)2
D.溶于水,溶液温度升高的物质:NaOH、浓H2SO4、NH4NO3
29.下列除杂试剂和方法使用错误的是
选项 | 物质(括号内为杂质) | 除杂试剂和方法 |
A | Cu(Fe2O3) | 加入稀硫酸,过滤 |
B | H2(水蒸气) | 通过浓硫酸,洗气 |
C | NaOH溶液(Na2CO3) | 加入石灰水,过滤 |
D | CaO(CaCO3) | 加入稀盐酸,过滤 |
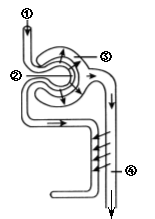
30.(乐山市中考化学)下列各组物质能在同一无色溶液中大量共存的是
A.BaCl2、KNO3、NaCl
B.H2SO4、KCl、FeCl3
C.NaOH、NaCl、HCl
D.AgNO3、ZnCl2、NaNO3
化 学 (35分)
六、填空题 (每空1分,共16分)
51.(4分)用数字和化学符号填空:
(1)2个氮原子_____________; (2)2个碳酸根离子______________;
(3)2个二氧化碳分子_______; (4)氧化铝中铝元素化合价为+3价________;
52.(5分)“凤凰”号火星探测器圆满完成任务,为人类探索火星提供了宝贵的科学资料。
(1)探测显示火星上存在液态水,下列说法错误的是_____________。
A.火星上的水与地球上的水化学性质不同
B.水是一种最重要的溶剂
C.水是生命活动必需的物质
(2)火星上含有丰富的镁、锰等资源。已知锰(Mn)的金属活动性在Al、Zn之间,且锰盐中锰元素的化合价为+2价,请写出一个有单质锰参加的置换反应(用化学方程式表示)__________________________。
(3)除火星外,部分其他行星也存在着“大气”(相当于地球上的空气),其主要成分为:
行星名称 | 冥王星 | 水星 | 木星 | 金星 |
大气成分 | 甲烷 | 没有气体 | 氨气、氦气、氢气、甲烷 | 二氧化碳、二氧化硫 |
根据表中信息,结合你所学过的知识回答:
①表中所列“大气”中含有稀有气体的行星是___________________;
②若金星上会下雨,那么此行星上最大的环境问题是_____________;
③甲烷是一种可燃性气体,但飞往冥王星上的火箭喷出的火焰去不能点燃冥王星上的甲烷,推测其原因是___________________________。
 53.(4分)人体缺乏维生素C(简写“Vc”)会患坏血病。右图所示为某种“维生素C”说明书的一部分,请回答:
53.(4分)人体缺乏维生素C(简写“Vc”)会患坏血病。右图所示为某种“维生素C”说明书的一部分,请回答:
(1)“Vc”属于______化合物(填“无机”或“有机”);
(2)若正常成人每天对“Vc”的最低需要量为60mg:
①当这些“Vc”完全来自右图的“维生素C”时,则每次服用“维生素C”至少______片;
②当这些“Vc”完全来自某种新鲜蔬菜(每1000g这种蔬菜含“Vc”120mg)时,每天至少应食用这种蔬菜_______g;
(3)取2片“维生素C”溶于水,滴入紫色石蕊试液变红色,说明“Vc”溶液的PH____7
(选填“>”、“<”或“=”)。
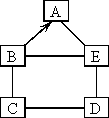 54.(4分)已知A、B、C、D、E分别是盐酸、硫酸铜溶液、氢氧化钠溶液、镁和氧化镁中的一种,它们之间的关系如图:一定条件下B可以生成A,其余相互连线的两种物质间能发生化学反应。
54.(4分)已知A、B、C、D、E分别是盐酸、硫酸铜溶液、氢氧化钠溶液、镁和氧化镁中的一种,它们之间的关系如图:一定条件下B可以生成A,其余相互连线的两种物质间能发生化学反应。
请回答:
(1)写出下列物质的化学式:B______ E_______
(2)写出C、D两种物质发生反应的化学方程式:_________
七、实验与探究 (每空1分,共13分)
55.(5分)实验室中,利用下列装置可以制取某些气体,请回答下列问题。
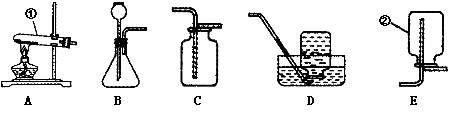
(1)写出图中标号仪器的名称:①____________ ②____________
(2)用大理石和稀盐酸反应制取CO2,应选用的发生装置是(填代号,下同)
____________,最好选用的收集装置是______________。
![]()
![]() (3)加热固体碳酸氢钠或固体碳酸氢铵都能产生CO2,其化学方程式分别是:
(3)加热固体碳酸氢钠或固体碳酸氢铵都能产生CO2,其化学方程式分别是:
①2NaHCO3 Na2CO3+H2O+CO2↑ ②NH4HCO3 NH3↑+H2O+CO2↑
某同学采用反应①的方法制取CO2,应该选用的发生装置是___________。
56.(6分)一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:
【查阅资料】硫酸铜溶液呈蓝色
【设计方案】(1)取少量黑色粉末于试管中![]() 观察现象
观察现象
实验中可能出现的现象与对应结论如下表,请你完成下表中①②相关内容:
现象 | 结论 |
溶液呈蓝色,有黑色不溶物 | 含CuO、C |
溶液颜色无明显变化,有黑色不溶物 | 只含① |
溶液呈蓝色,② 。 | 只含CuO |
 (2)通过实验及分析,确定该粉末为氧化铜和炭粉
(2)通过实验及分析,确定该粉末为氧化铜和炭粉
的混合物,为了进一步探究它们的性质,探
究小组又利用这种混合物补充做了如下图所
示实验:
①能证明CuO与C已发生化学反应的实验现象是
a ,b 。试管b中反应的化学方
程式为 。
②最能说明a试管中物质已完全反应的实验现象是
八、计算题 (共6分)
57(乐山市中考化学).课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
| 实验一 | 实验二 | 实验三 | 实验四 |
原固体混合物质量 | 10g | 10g | 10g | 10g |
加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
生成的沉淀的质量 | 2g | m | 5g | 5g |
请分析表中数据回答并计算[(4)要求写计算过程 ]
(1)10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为 g。
(2)m= g。
(3)原固体混合物中Na2CO3的质量分数是多少?
乐山市中考化学参考答案
一、选择题(每小题2.5分,共35分)
题号 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 |
答案 | D | D | C | A | B | D | D | A | D | C |
题号 | 27 | 28 | 29 | 30 |
|
|
|
|
|
|
答案 | B | D | D | A |
|
|
|
|
|
|
二、填空题(每空各1分 共16)
51.(1) 2N; (2) 2 CO32—; (3)2CO2;(4)![]() 2O3;
2O3;
52.(1) A
(2)Mn+ZnCl2 == Zn + MnCl2 ( 其它合理答案均可,下同)
(3)①木星 ②易形成酸雨(其他答案合理也可)③冥王星上缺少氧气
53. (1)有机 (2) ① 2 片 ② 500克 (3) <
54.(1)Mg; HCl (2)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
三、实验探究题(每空各1分 共11分)
55.(1)试管 集气瓶
(2)B C
(3)A
56. (1) ① C ②无黑色不溶物
(2)①a: 黑色粉末中有红色粉末出现(其他合理答案也可)
b : b试管内澄清的石灰水变浑浊
化学方程式 C+2CUO![]() 2CU + CO2↑
2CU + CO2↑
②黑色粉末全部变成红色粉末
四、计算题(8分)
57.(1) 5 (2) 4
(3)解:设10克原固体混合物中含Na2CO3的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g
![]()
![]() =
= ![]()
![]()
x= 5.3g
则原固体混合物中Na2CO3的质量分数为:5.3g/10g x100%=53%
答:原固体混合物中Na2CO3的质量分数为53%

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...