由于格式问题此试题可能会出现乱码的情况
为了方便您阅读请点击右上角的全屏查看
2018内江市中考化学冲刺试题
相对原子质量:H ---1 C----12 O----16 Na----23 Cl----35.5
一、选择题(共48分,每题4分,每题只有一个正确答案)
1、下列生活中的常见现象,一定含有化学变化的是( )
A.铁栅栏生锈 B.霓虹灯闪烁 C.樟脑球升华 D.活性炭除臭
2、下列叙述属物质的物理性质的是( )
A.沙子能够制造出芯片和光导纤维 B.水的密度是1g/cm3
C.锌粒遇盐酸能产生气体 D.葡萄能酿酒
3、蜡烛的主要成分是石蜡,刚熄灭时,烛芯会冒出一缕白烟,燃着的火柴只碰到白烟,白烟可燃烧并引燃蜡烛。则此白烟可能是( )
A.氮气 B.水蒸气
C.二氧化碳 D.石蜡蒸汽冷凝的固体小颗粒
4、如图所示,实验操作正确的是( )
A.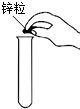 B.
B.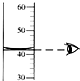
C.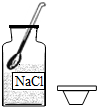 D.
D.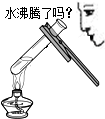
5、(内江市中考化学)下图是表示气体分子的示意图,图中:“●”和“○”分别表示两种不同质子数的原子,其中表示化合物的是( )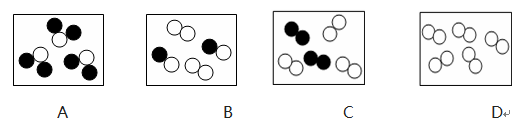
6、某同学用分子的观点解释下列现象。其中错误的是( )
A.热胀冷缩──分子大小随温度的变化而改变
B.花香四溢──分子不停地运动
C.食物腐败──分子本身发生了变化
D.酒精挥发──分子间间隔变大
7、下列关于水的叙述不正确的是( )
A.水是一种最常用的溶剂 B.煮沸能降低水的硬度
C.用肥皂水鉴别硬水和软水 D.电解水的负极产生氧气
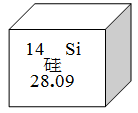 8、下图是硅元素在周期表中的一格,依据图中的信息得到的下列认识错误的是( )
8、下图是硅元素在周期表中的一格,依据图中的信息得到的下列认识错误的是( )
A.该元素原子的质子数为14
B.该元素的相对原子质量为28.09
C.该元素一个原子的原子核外有14个电子
D.该元素属于金属元素
9、Na2FeO3是一种绿色、无污染的净水剂。则其中铁元素的化合价为( )
A.+2 B.+3 C.+4 D.+6
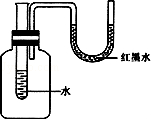
10、如图所示向试管里的水中加入某种不与水发生化学反应的物质后,原来U型管内两端在同一水平上的红墨水,右边液面降低些,左边的液面上升了些,则加入的物质可能是( )
A.活性炭 B.氯化钠 C.硝酸铵D.氢氧化钠
11、下列有关饱和溶液的说法中,正确的是( )
A.饱和溶液的溶质质量分数一定比不饱和溶液的大
B.饱和溶液降温析出晶体后的溶液一定是不饱和溶液
C.任何饱和溶液升温后都会变成不饱和溶液
D.一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液
12、我省盛产茶叶,“雪青”“清润名茶”等绿茶享誉省内外.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46.下列说法不正确的是( )
A.单宁酸由碳、氢、氧三种元素组成
B.1个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸分子中碳、氢、氧原子数比38:26:23
D.1个单宁酸分子中含26个氢分子
二、(内江市中考化学)填空题(24分,每空3分)
13、用数字或化学符号填空:
(1) 两个铁离子 ___________________
(2)3H2O中“2”表示的意义:________________
14、如图中的①、②是氟元素、钙元素在元素周期表中的信息,A.B.C.D是四种粒子的结构示意图.请你回答: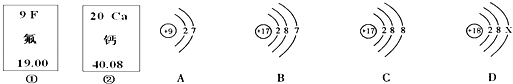
(1)A.B.C.D属于同种元素的粒子是 (填序号);
(2)A粒子的化学性质与B.C.D中哪一种粒子的化学性质相似 (填序号)
15、在横线填上相应的物质序号:
在下列物质中:①洁净的空气 ②硬水 ③氢气 ④液态氧 ⑤冰水共存物 ⑥氯酸钾 ,用序号填空:
(1)其中属于纯净物的是______________ ,(2)属于化合物的是 ___________,
16、水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水。
(1)我国规定生活饮用水的水质必须达到下述四项指标:
a.不得呈现异色
b.不得有异味
c.应澄清透明
d.不得含有细菌和病毒。
其中“c指标”可以通过 操作达到。
(2)有些地区还在使用硬水作为饮用水,可以通过 的方法降低水的硬度。
三、实验题(每空3分,共18分)
14、欲配制50 g质量分数为15%的NaCl溶液,下图是某同学配制溶液的操作过程。
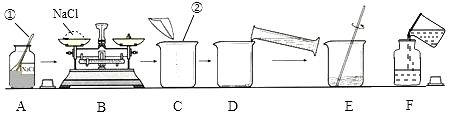
(1)写出标号仪器的名称:①______________
(2)B操作中应称量NaCl的质量是________g;若称量时错把氯化钠放到了右盘(1 g以下用游码),其他过程没有误差,则实际配制的NaCl溶液的溶质质量分数是___________。
(3)所需量取水的体积为__________(水的密度为1 g/cm3),量筒的规格应为___________(填“10 mL”或“50 mL”)。
(4)F操作中溶液洒落可能导致溶质质量分数无影响。但D操作时有少量水溅出可能导致溶质质量分数偏高。量取水时仰俯视读数可能导致溶质质量分数__________________________(填“偏高”“偏低”或“无影响”,下同)
四、计算题(10分)
 18、 葡萄糖(化学式:C6H12O6)是生命体所需要能量的主要来源.有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请计算:
18、 葡萄糖(化学式:C6H12O6)是生命体所需要能量的主要来源.有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请计算:
(1)配制这瓶葡萄糖溶液,需要固体葡萄糖的质量为:_______________ g.
(2)要把这瓶葡萄糖溶液加水稀释为2%的葡萄糖溶液,需要水的质量为多少?(写出计算过程)
化学B卷 (30分)
19、填空题(12分)
元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分.
族 | IA |
| 0 | |||||
1 | 1H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He |
2 | 3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne |
3 | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar |
(1)查出碳的相对原子质量: ,画出氯离子的结构示意图 .
(2)11号元素和16号元素形成化合物的化学式为__________________
(3)表中不同种元素最本质的区别是 (填序号)
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期.近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为 .
(5)周期表中每一个横行叫做一个周期,第三周期开头元素和靠近尾部的元素
的原子结构示意图分别为![]() 和
和![]() ,它们的单质易发生如图所示变化:
,它们的单质易发生如图所示变化:
根据以上信息,可以得到的结论是 _____________________________________ .
20、(内江市中考化学)探究题(12分)
 某化学兴趣小组的同学对有关氧气方面进行探究
某化学兴趣小组的同学对有关氧气方面进行探究
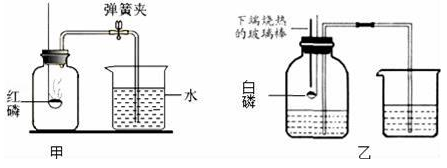
探究一:对空气中氧气含量的测定实验进行探究:
(1)如图甲所示装置和药品进行实验,集气瓶中发生反应的文字或符号表达式为 _______________________________ 。
(2)该组同学做了6次实验,整理数据如下:
| 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
(注:集气瓶容积为100mL)通过6次实验,该组同学探究出氧气约占空气体积的 ________________________________________ 。
(3)小林同学利用甲图装置测定空气中氧气的含量,下列操作会使测定结果偏小的是 ( )
A、实验装置可能漏气
B、实验中所取的红磷过量
C、实验前没有将弹簧夹夹紧
D、红磷燃烧结束后,没等装置冷却就打开弹簧夹
(4)小组内同学查阅资料后知道白磷40℃即燃烧,燃烧产物与红磷相同,于是采用改进后的乙装置进行重新探究.主要操作是:在实际容积为100mL的集气瓶里先装进30mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃.
①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是 ___________________ ,若实验非常成功,最终集气瓶中水的体积约为 _________________________ mL.
②你认为集气瓶里预先装进的水有哪些作用? ( ) (填序号)
a.加快集气瓶冷却 b.液封导气管末端以防气体逸出 c.缓冲集气瓶内气压的骤然升高
21、计算题 (6分,每小题2分)
钠摄入过量或钾摄入不足都是导致高血压的风险因素.日常生活中选择食用低钠盐能实现减钠补钾.如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
(1)溶剂水中氢元素与氧元素的质量为 .(最简整数比)
(2)人体每天摄入钠元素的质量不宜超过2.3g.如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(写出计算过程,结果保留一位小数)

一、选择题(共48分,每题4分)
1、A 2、 B 3、 D 4、 B 5、 A 6、A 7、 D 8、D 9、 C 10、C 11、D 12、D
二、填空题(24分,每空3分)
13、(1)2Fe3+ (2)一个水分子中有2个氢原子 14、BC B
15、(1)③④⑤⑥;(2)⑤⑥ 16、(1)过滤 (2)煮沸
三、实验题(每空3分,共18分)
17、(1)药匙 (2)7.5 13.3% (3)42.5 mL 50 mL (4) 偏低
四、计算题(10分)
18、(1)25 (2)750g
化学B卷 (30分)
19、12.01 Na2S A 118
在化学反应中,金属元素的原子比较容易失去最外层的电子,非金属元素的原子比较容易得到电子,得到最外层电子数目为8的稳定结构
20、 (1) P + O2 点燃 P2O5 (2) 20%或1/5 (3) AD
(4) 先下降后上升 44 ab
21、 解:(1)1:8
(2):设 一个人每天摄入该品牌低钠盐不宜超过的质量x
x×70%×(23/58.5)=2.3g
x=8.4g
答:一个人每天摄入该品牌低钠盐是质量不宜超过8.4g.

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...