此试题可能存在乱码情况,在查看时请点击右上角全屏查看
2018年北海中考化学冲刺试题
一、我会选择(共14小题,每小题3分,满分42分)
1. 下列变化中,发生了化学变化的是( )
| A. | 海水晒盐 | B. | 饭菜变馊 | C. | 酒精挥发 | D. | 冰雪融化 |
2.图中所示的实验操作中,正确的是( )
A.给液体加热 B.放入铁钉 C.用灯帽熄灭酒精灯 D.测溶液的酸碱度 |
3.下列物品所含的主要材料,不属于合成材料的是( )
| A. | 涤纶衣 | B. | 塑料杯 | C. | 铁桶 | D. | 尼龙袜 |
4. Cl的原子结构示意图为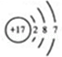 ,下列关于Cl的说法错误的是( )
,下列关于Cl的说法错误的是( )
| A. | 电子层数是3 |
| 核内质子数是17 |
| C. | 最外层电子数是7 | D. | 在化学反应中易失电子 |
5. 6月5日为“世界环境日”,今年我国的主题是“践行绿色生活”.下列做法符合这一主题的是( )
|
| 倡导使用节能灯 | B. | 使用一次性筷子 |
| C. | 随意排放生活污水 | D. | 随便丢弃废电池 |
6. 下列物质中能使紫色石蕊试液变红的是( )
| A. | 二氧化碳 | B. | 食盐水 | C. | 烧碱 | D. | 熟石灰 |
7. 区分稀硫酸和稀盐酸,不能使用的试剂是( )
| A. | Ba(NO3)2 | B. | BaCl2 | C. | Ba(OH)2 | D. | NaCl |
8.化学与人类生活、社会生产密切相关.下列说法不正确的是( )
A.常吃海产品、肝脏、奶类、豆类、小米等食物,以补充人体必需的锌等微量元素
B.利用和开发太阳能、风能、核能等新能源,以节约化石燃料,有效减少碳排放
C.学生在食堂多用自带饭盒打饭,尽量少用一次性用品,少叫外卖.以节约资源,保护环境
D.为使植物的茎叶生长茂盛,提高粮食产量.大量使用尿素[CO(NH2)2]等化学肥料
9. 下列有关物质的用途错误的是( )
A.用稀盐酸清除铁锈 B.蒸馒头用食盐作发酵粉
C.用稀有气体制作霓虹灯 D.用熟石灰改良酸性土壤
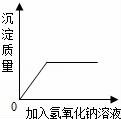
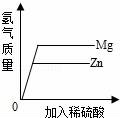
10.下列实验过程中与图象描述相符的一组是( )
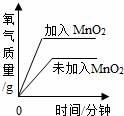
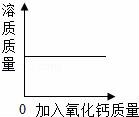
A. 两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生
B. 向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液
C. 向等质量的镁、锌中分别加入稀硫酸
D. 室温下,向一定质量的饱和石灰水中加入氧化钙
11.有一种生活中常见的燃料,现在取这种燃料2.3g在足量氧气中充分燃烧,生成4.4g二氧化碳和2.7g水,则你认为该燃料可能是
A.C2H4 B.CH4 C. C2H5OH D.C2H6
12. 下列所用试剂能达到实验目的是( )
| 实验目的 | 试剂 | ||||||||
A | 鉴别浓硫酸与稀硫酸 | 木条 | ||||||||
B | 鉴别氯化钡溶液与氯化钙溶液 | 碳酸钾溶液 | ||||||||
C | 除去氮气中的氧气 | 水 | ||||||||
D | 除去二氧化碳中的一氧化碳 | 氢氧化钠溶液 | ||||||||
| A. | A | B. | B | C. | C | D. | D | ||
13. 下列各组溶液混合,能发生化学反应,并且一定能得到无色透明溶液的是
A.CuCl2、KOH、NaCl B.NaCl、HCl、K2CO3
C.KOH、KMnO4、H NO3 D.MgCl2、AgNO3、NaOH
14.下图是金元素在元素周期表中的信息示意图。从图中获取的信息正确的是

A.金元素属于非金属元素 B.一个金原子的中子数为197
C.一个金原子的核外电子数为118 D.一个金原子中粒子总数为276
二、我会填空(共3小题,16分)
15.(4分)请用化学符号填空
(1)钙离子 ;(2)2个磷原子 (3)天然气 ;(4)2个三氧化硫分子 .
16.(6分)2016年3月22日是第二十四届“世界水日”。水与人类的生活和生产密切相关,请回答下列问题:
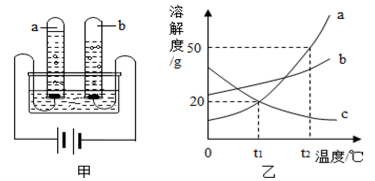
⑴图甲是水通电分解的实验装置图。该实验中,试管a中产生的气体是 ,检验方法 。
⑵高层建筑物发生火灾时,消防队员常用高压水枪灭火,灭火原理是 。
⑶图乙为a、b、c三种物质的溶解度曲线,请根据图乙回答下列问题:
①t1°C 时,将20g物质c加入到50g水中,充分搅拌后,所得溶液质量为 g。
②t2°C时,将a、b的饱和溶液降温至t1°C,析出晶体的质量 (填字母)。
A.a多 B.b多 C.一样多 D.无法判断
③将t2°C时a、b、c三种物质的饱和溶液降温到t1°C,所得溶液的溶质质量分数大小关系为 。A.b>a=c B.b>a>c C.a>b>c D.无法判断
17.(6分)人类的生产和生活都离不开金属
(1)生铁和钢中最主要的元素是 ;用铝壶烧水主要利用铝具有良好的 性.
(2)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的 .
(3)验证Zn、Cu、Ag的金属活动![]() 性顺序
性顺序![]() ,可选择的试剂
,可选择的试剂![]() 是 (填字母序号)
是 (填字母序号)
A.Zn、Ag、CuCl2溶液 B.Cu、Ag、ZnSO4溶液
C.Zn、Cu、Ag、稀硫![]() 酸 D. Zn、Cu、AgNO3溶液.
酸 D. Zn、Cu、AgNO3溶液.
(4)微型化录音录像的高性能带中磁粉主要材料之一是化学组成相当于CoFe2O4的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,则铁元素的化合价为 ;
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤液中一定不含有的物质是 .
三、我会解答(共2小题,12分)
18.(6分)A在纯净的B中点燃后燃烧生成C和D,A、B、C、D的微观示意图如下所示
物质 | A | B | C | D |
|
分子示意图 |
|
|
|
|
看图回答:
(1)属于氧化物的是 (填字母序号)
(2)A中氮、氢原子数之比为 ,氮、氢元素质量之比为 .
(3)A在B中充![]() 分燃烧的化学方程式为 ,基本反应类型为 .
分燃烧的化学方程式为 ,基本反应类型为 .
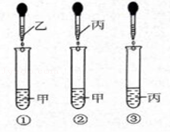
19.(6分)甲、乙、丙、丁都是初中化学中最常见的物质,已知它们由H、O、C、Cl、Na、Ca 6种元素中的2种或3种组成,丙与甲、乙、丁都能发生反应.将这四种物质的溶液按图所示相互滴加,现象为:①产生白色沉淀;②有气泡冒出;③无明显现象
(1)甲、乙、丙、丁都属于 (填“单质”或“化合物”).
(2)试管②中产生的气体是 (填化学式).
(3)试管①中反应的化学方程式是 .
(4)向试管③滴加的溶液溶质可能是 (填化学式,下同)或 ![]() .
.
四.我会实验(22分)
20.(8分).根据下列所给的实验装置回答有关问题
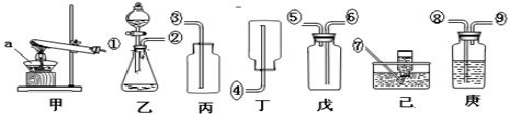
回答下列问题:
⑴甲装置中a仪器的名称是 ,庚装置能起干燥作用瓶中装 。
⑵小王在实验操作考查中抽到的考题是“在实验室制取一满瓶干燥二氧化碳,放置在实验桌上。”为完成实验,他应选用上列装置,从左到右的连接顺序为 (填接口序号)。请写出反应的化学方程式 ;检验集气瓶是否收集满二氧化碳的方法是 。
(3)经过学习小明对气体制备有一些心得,如:选择制取气体的反应装置时应考虑的两个因素是 , 。
21.(14分)在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察![]() 到以下异常实验现象:
到以下异常实验现象:
实验序号 | 滴加Cu | 实验现象 |
① | 第1﹣6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
② | 第7﹣9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式 .
实验①中蓝色沉淀为什么消失?同学们继![]() 续进行如下探究.
续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃﹣80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是 .
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
实验序号 | 实验方法与操作 | 实验现象 | 结论 |
③ | 将少许Cu(OH)2粉末加到 |
| 猜想一错误 |
④ |
|
| 猜想二正确 |
【结论与反思】(1)根据实验,并进一步查阅资料知道,Cu(OH)2在NaOH溶液中溶解生成Na![]() 2Cu(OH)4,反应的化学方程式是
2Cu(OH)4,反应的化学方程式是
(2)根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是 .
五.我会实验(8分)
22.下列五种溶液:①NaOH 溶液、 ②Ba(OH)2溶液、③Na2SO4溶液、④稀硝酸、⑤混有少量硝酸的MgSO4溶液
(1)指出其中属于碱溶液的 (选填序号);
(2)若将20%的Ba(OH)2溶液与Na2SO4溶液混合,产生沉淀质量是116.5克.需要20%的硫酸钠溶液多少克?这时所得溶液的溶质质量分数是多少?
2018年北海中考化学冲刺试题参考答案
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
B | C | C | D | A | A | D | D | B | C | C | A | B | D |
15、(1)Ca2+;(2)2P;(3)CH4;(4)3SO3.
16、(1)O2 用带火星的木条检验,木条复燃,证明是氧气 (2)降低温度到着火点以下(3)①60②D③B
17、(1)铁元素 导热 (2)氧化铝保护膜 (3)A(4)+3(5) 硫酸和硫酸铜
![]()
18、(1)C;(2)1:3,14:3;(3)4NH3+3O2 ==== 2N2+6H2O,置换反应
19、(1)化合物;(2)CO2;(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(4)NaOH,Ca(OH)2.
20.(1)酒精灯 ; 浓硫酸
(2)②⑧⑨③或)②⑧⑨⑥⑤ ; CaCO3+2HCl=CaCl2+2H2O+CO2↑;用燃着的木条放到集气瓶口,木条熄灭,证明已集满
(3)反应物的状态;反应条件
21、CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可);
实验序号 | 实验方法与操作 | 实验现象 | 结论 |
③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 |
沉淀不消失 | 猜想一错误 |
④ |
将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 |
沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
Cu(OH)2+2NaOH=Na2Cu(OH)4;
资料Ⅰ显示Cu(OH)2在室温下稳定,70℃﹣80℃时可脱![]() 水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观
水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观![]() 察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
22(1)①②
(2)355g
6%

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...