2017-2018年惠州市九年级第二次月考化学试题【免费版含答案】
由于版式的问题,试题可能会出现乱码的现象,为了方便您的阅读请点击全屏查看
一、化学选择题:(每题只有一个正确答案,共45分)
1.下列物质的变化过程中,不涉及化学变化的是()
A.光合作用 B.人的呼吸
C.节日燃放焰火 D.用活性炭净化水
2.1元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的.在讨论时,有同学提出:“我们可以先拿磁铁来吸一下”.就“拿磁铁来吸一下”这一过程而言,属于科学探究中的()
A.实验 B.假设 C.观察 D.做结论
3.自来水厂净水流程为:天然水→沉降→过滤→吸附→自来水,其中常用作除去臭味的试剂是()
A.漂白粉 B.明矾 C.氯气 D.活性炭
4.下列实验操作正确的是()
A. B.
B. C.
C.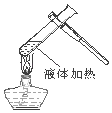 D.
D.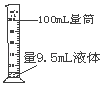
5.下面是从小芳同学笔记中摘录的部分化学用语,你认为正确的是()
A.碳酸钾:KCO3 B.2个二氧化碳分子:2 CO2
C.氯化锌:ZnCl D.镁离子:Mg+2
6.是某原子的结构示意图,以下说法正确的是()

A.该原子的元素符号为X B.该原子核外电子总数为4
C.木炭中含有该原子 D.该种元素属于金属元素
7.根据下列原子结构示意图判断,化学性质最稳定的是()
A.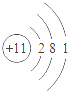 B.
B.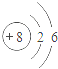 C.
C.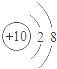 D.
D.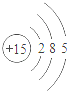
8.元素M在化合物中只有一种化合价,下列化学式有错误的是()
A.M(OH)2 B.MCl3 C.M2(SO4)3 D.M2O3
9.根据组成元素的类别,对下列氧化物分类,其中﹣种与另外三种不属于同一类别,它是()
A.MnO2 B.Cu2O C.P2O5 D.Fe3O4
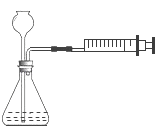
10.实验室可用如图装置制氧气,可用推拉注射器的方法检验装置的气密性,当缓慢拉活塞时,如果装置气密性良好,可观察到()
A.注射器内进入液体 B.瓶内液面上升
C.长颈漏斗内的液面上升 D.长颈漏斗下端管口产生气泡
11.有关尿素[CO(NH2)2]的说法正确的是()
A.尿素的相对分子质量为:12+16+14+1×2×2=46
B.一个尿素分子中碳、氧、氮、氢四种原子的个数比为1:1:2:4
C.尿素中碳、氧、氮、氢四种元素的质量比为:12:16:14:1
D.尿素中氮元素质量分数的计算式为:![]() ×l00%
×l00%
12.“绿色亚运”拒绝兴奋剂,乙基雌稀醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O,下列关于乙基雌稀醇的说法正确的是()
A.它属于氧化物
B.一个分子中含有16个H2单质
C.分子中C、H两种元素的质量比是5:8
D.它由三种元素组成
13.根据下列各组原子结构示意图,元素的化学性质相似的一组是()
A.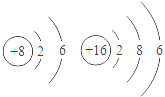 B.
B.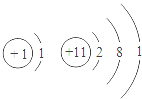 C.
C.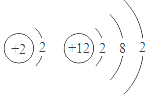 D.
D.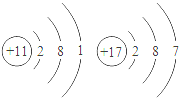
14.亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒.区别它们的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种具有刺激性气味气体的是亚硝酸钠.该气体可能是()
A.NH3 B.SO2 C.NO2 D.N2
15.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是()
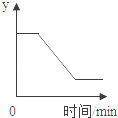
A.生成O2的质量 B.固体中MnO2的质量
C.固体中氧元素的质量 D.固体中钾元素的质量分数
二、化学填空题:(共45分)
16.根据下列几种粒子的结构示意图,回答下列问题

(1)其中属于阴离子是 (填序号,下同);
(2)具有相似化学性质的是 ;
(3)属于同种元素的是 .(4)钠离子符号
(5)由氧原子变成氧离子发生的是 变化,理由是 .
17.某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
(1)甲同学选用如右图所示的装置制取氧气.
①写出仪器B的名称: .
②甲同学应选取的试剂是Mn02和 (填化学式),Mn02固体在该反应中起 作用.
③除用排水法外,甲同学还可选择 法收集氧气.
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现.该实验操作的目的是 .
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为 .实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2Mn04分解放出O2做出上述猜想的理由是 .
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后 测得Mn02的质量不变.则猜想 错误.
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得
出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 .
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物K2O对其分 解产生影响.请设计实验方案验证: .
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识? .
18.3月22日是“世界水日”.关于水的知识,请回答下列问题:
(1)下列净水方法中,生产自来水使用的方法有(填字母序号) ;
A.沉淀B.过滤C.煮沸D.蒸馏E.吸附
(2)实验室常用过滤的方法对液体进行提纯,在此操作中需要用到的玻璃仪器有:玻璃棒、烧杯、 (填仪器名称);生活中常用 的方法将硬水软化.
(3)有关水的组成和结构的叙述中,正确的是(填字母序号) ;
A.水是由水分子构成的
B.水分子的相对分子质量是18g
C.水中氢、氧元素的质量比为2:1
D.水分子是由氢原子和氧原子构成的
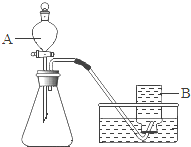
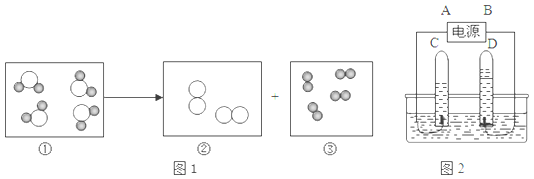
(4)下列图1示意图①~③中,“![]() ”表示氢原子,“
”表示氢原子,“![]() ”表示氧原子.表示化合物的是(填序号) ,③所代表的物质是图中 试管 (填字母) 中产生的气体,图2中A是电源的 (填“正”或“负”)极.
”表示氧原子.表示化合物的是(填序号) ,③所代表的物质是图中 试管 (填字母) 中产生的气体,图2中A是电源的 (填“正”或“负”)极.
(5)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,写出该反应的符号表达式 .
三、计算题:(共10分)
19.(10分)蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收.丙氨酸(化学式为C3H7O2N)就是其中的一种.请回答下列问题:
(1)丙氨酸分子中C、H、O、N各原子个数比为 .
(2)丙氨酸的相对分子质量是 ,氮元素的质量分数为 (计算结果精确到0.1%).
2017-2018年惠州市九年级第二次月考化学试题参考答案与试题解析
一、选择题:(每题只有一个正确答案,共45分)
1.下列物质的变化过程中,不涉及化学变化的是()
A.光合作用 B.人的呼吸
C.节日燃放焰火 D.用活性炭净化水
【分析】有新物质生成的变化叫化学变化,光合作用、人的呼吸、节日燃放焰火都属于化学变化;没有新物质生成的变化叫物理变化.化学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有新物质生成.
【解答】解:A、光合作用生成氧气等物质,属于化学变化,故选项错误;
B、人的呼吸呼出二氧化碳等物质,属于化学变化,故选项错误;
C、节日燃放焰火生成有害气体和烟尘,属于化学变化,故选项错误;
D、用活性炭净化水,没有新物质生成,属于物理变化,故选项正确;
故选D
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决.本考点主要出现在选择题和填空题中.
2.1元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的.在讨论时,有同学提出:“我们可以先拿磁铁来吸一下”.就“拿磁铁来吸一下”这一过程而言,属于科学探究中的()
A.实验 B.假设 C.观察 D.做结论
【分析】科学探究的主要环节有提出问题、猜想与假设、制定计划与设计实验、进行实验与收集证据、分析与论证、评估、交流与合作.
【解答】解:利用磁铁吸引铁的性质,“拿磁铁来吸一下”这一过程是科学探究中的进行实验环节.
故选A.
【点评】此题是对科学探究环节的考查,解题的关键是对采用过程的分析,并结合科学探究的基本过程解决此题.
3.自来水厂净水流程为:天然水→沉降→过滤→吸附→自来水,其中常用作除去臭味的试剂是()
A.漂白粉 B.明矾 C.氯气 D.活性炭
【分析】根据常用的净水剂的性质分析.活性炭具有吸附性,漂白粉、氯气具有消毒杀菌的作用,明矾是一种絮凝剂.
【解答】解:A、漂白粉具有消毒杀菌的作用.故A不符合题意;
B、明矾是一种絮凝剂,加快沉降的速率.故B不符合题意;
C、氯气具有消毒杀菌的作用.故C不符合题意;
D、活性炭具有吸附性,常用作除去臭味的试剂.故D符合题意.
故选D.
【点评】本题考查了净水的知识,完成此题,可以依据物质的性质进行.
4.下列实验操作正确的是()
A. B.
B.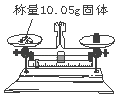 C.
C. D.
D.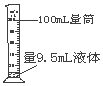
【分析】A、根据酒精灯的使用方法进行分析判断.
B、根据托盘天平的使用方法进行分析判断.
C、根据给试管中的液体加热的方法进行分析判断.
D、根据量筒的使用原则进行分析判断.
【解答】解:A、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误.
B、用天平称量药品时要左物右码,托盘天平只能精确到0.1g,不能称量10.05g固体,图中所示操作错误.
C、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积![]() ,图中所示操作正确.
,图中所示操作正确.
D、量筒量程选择的依据有两点:一是保证量取一次,二是量程与液体的取用量最接近,量取9.5mL的液体,10mL量筒能保证量取一次,且量程与液体的取用量最接近,误差最小;不能使用100mL的量筒量取9.5mL的液体,图中所示操作错误.
故选C.
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.
5.下面是从小芳同学笔记中摘录的部分化学用语,你认为正确的是()
A.碳酸钾:KCO3 B.2个二氧化碳分子:2 CO2
C.氯化锌:ZnCl D.镁离子:Mg+2
【分析】A、碳酸钾中钾元素显+1价,碳酸根显﹣2价,组成其化学式即可.
B、分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
C、氯化锌中锌元素显+2价,氯元素显﹣1价,组成其化学式即可.
D、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
【解答】解:A、碳酸钾中钾元素显+1价,碳酸根显﹣2价,其化学式为:K2CO3,故选项化学用语书写错误.
B、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个二氧化碳分子可表示为:2CO2,故选项化学用语书写正确:.
C、氯化锌中锌元素显+2价,氯元素显﹣1价,根据化合价原则,其化学式为:ZnCl2,故选项化学用语书写错误.
D、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;镁离子可表示为:Mg2+,故选项化学用语书写错误.
故选B.
【点评】本题难度不大,主要考查同学们对常见化学用语(原子符号、分子符号、化学式、离子符号等)的书写和理解能力
6.是某原子的结构示意图,以下说法正确的是()
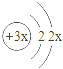
A.该原子的元素符号为X B.该原子核外电子总数为4
C.木炭中含有该原子 D.该种元素属于金属元素
【分析】由题意,根据某原子的结构示意图,结合“质子数=原子核外电子数=核电荷数”,可求得x的值,从而判断该元素名称、符号.
【解答】解:根据某原子的结构示意图,结合“质子数=原子核外电子数=核电荷数”,则3x=2+2x,解得x=2,故质子数为6的元素为碳元素,元素符合为“C”;该原子核外电子总数为“6”;木炭为碳的单质,故含有碳原子;该元素为“非“金属元素.
故选C.
【点评】了解原子结构示意图与离子结构示意图的区别;掌握原子的定义和构成.
7.根据下列原子结构示意图判断,化学性质最稳定的是()
A.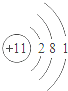 B.
B.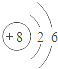 C.
C.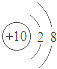 D.
D.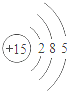
【分析】化学性质由粒子结构的最外层电子数决定,如果一个电子层,最外层电子数为2已达稳定;如果2个以上电子层,最外层电子数为8,则达稳定结构.观察题目中的粒子结构示意图的最外层电子数特点,可知其答案.
【解答】解:A、该粒子最外层电子数为1,易失去电子而达稳定结构,故A不符合题意;
B、该粒子最外层电子数为6,易得到电子而达稳定结构,故B不符合题意;
C、该粒子最外层电子数为8,已达稳定结构,化学性质最稳定,故C符合题意;
D、该粒子最外层电子数为5,没有达到稳定结构,故D不符合题意.
故选C.
【点评】了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点.
8.元素M在化合物中只有一种化合价,下列化学式有错误的是()
A.M(OH)2 B.MCl3 C.M2(SO4)3 D.M2O3
【分析】根据题意,元素M在化合物中只有一种化合价,结合在化合物中正负化合价代数和为零,进行分析解答.
【解答】解:A.氢氧根显﹣1价,设M元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣1)×2=0,则x=+2价.
B.氯元素显﹣1价,设M元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(﹣1)×3=0,则y=+3价.
C.氯元素显﹣1价,设M元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:z+(﹣1)×3=0,则z=+3价.
D.氧元素显﹣2价,设M元素的化合价是w,根据在化合物中正负化合价代数和为零,可得:2w+(﹣2)×3=0,则w=+3价.
故选A.
【点评】本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.
9.根据组成元素的类别,对下列氧化物分类,其中﹣种与另外三种不属于同一类别,它是()
A.MnO2 B.Cu2O C.P2O5 D.Fe3O4
【分析】根据氧化物中组成元素的类别考虑(从金属元素和非金属元素方面考虑).
【解答】解:A、B、D均属于金属氧化物,C属于非金属氧化物;故C与另外三种不属于同一类别.
故选C.
【点评】本题难度不大,主要考查氧化物质的分类,氧化物可分为金属氧化物和非金属氧化物.
10.实验室可用如图装置制氧气,可用推拉注射器的方法检验装置的气密性,当缓慢拉活塞时,如果装置气密性良好,可观察到()
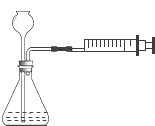
A.注射器内进入液体 B.瓶内液面上升
C.长颈漏斗内的液面上升 D.长颈漏斗下端管口产生气泡
【分析】根据检查装置气密性的原理分析即可.装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏.
【解答】解:向外拉活塞时锥形瓶中气体体积减小,外界大气压迫使外边的空气通过长颈漏斗进入锥形瓶,从而观察到长颈漏斗下端口有气泡冒出.
故选D
【点评】装置气密性的检验是常考的实验题,也是难点,这需要同学们在做这类题时多总结,多思考,这类题目不要死记硬背,关键是理解,等同学们见的这类题多了,问题自然就会迎刃而解.同学们需要注意,检验装置气密性时可以通过两种方法来改变体系内的压强,①升温:用手掌捂热装置或用酒精灯微热装置②充气:常用注射器充气③抽气:常用注射器抽出装置中的一部分气体.同学们可以根据不同的实验装置来选择恰当的方法.
11.有关尿素[CO(NH2)2]的说法正确的是()
A.尿素的相对分子质量为:12+16+14+1×2×2=46
B.一个尿素分子中碳、氧、氮、氢四种原子的个数比为1:1:2:4
C.尿素中碳、氧、氮、氢四种元素的质量比为:12:16:14:1
D.尿素中氮元素质量分数的计算式为:![]() ×l00%
×l00%
【分析】A、根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析判断.
B、根据1个尿素分子的构成,进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数=![]() ×100%,进行分析判断.
×100%,进行分析判断.
【解答】解:A、尿素的相对分子质量为12+16+(14+1×2)×2=60,故选项说法错误.
B、一个尿素分子是由一个碳原子、一个氧原子、两个氮原子、四个氢原子构成的,则尿素中碳原子、氢原子、氧原子、氮原子的个数比为1:1:2:4,故选项说法正确.
C、尿素中碳、氧、氮、氢四元素的质量比为12:16:(14×2):(1×2×2)=3:4:7:1,故选项说法错误.
D、尿素中氮元素质量分数的计算式为![]() ×100%,故选项说法错误.
×100%,故选项说法错误.
故选:B.
【点评】本题难度不大,考查同学们灵活运用化学式的含义、有关计算进行分析问题、解决问题的能力.
12.“绿色亚运”拒绝兴奋剂,乙基雌稀醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O,下列关于乙基雌稀醇的说法正确的是()
A.它属于氧化物
B.一个分子中含有16个H2单质
C.分子中C、H两种元素的质量比是5:8
D.它由三种元素组成
【分析】A、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B、根据分子是由原子构成的进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据乙基雌稀醇化学式的含义进行分析判断.
【解答】解:A、乙基雌稀醇是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误.
B、分子是由原子构成的,一个分子中含有32个原子,不含H2单质,故选项说法错误.
C、分子中C、H两种元素的质量比是(12×20):(1×32)=15:2,故选项说法错误.
D、乙基雌稀醇是由碳、氢和氧三种元素组成的,故选项说法正确.
故选D.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
13.根据下列各组原子结构示意图,元素的化学性质相似的一组是()
A.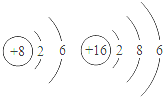 B.
B. C.
C.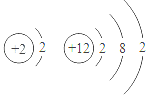 D.
D.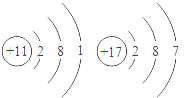
【分析】元素的化学性质取决于该元素原子的最外层电子数,最外层电子数小于4,易失电子;最外层电子数大于4,易得电子;最外层电子数为8(He除外),性质稳定.
【解答】解:
A、两种元素的原子最外层均为6个电子,都易得2个电子而形成8电子稳定结构,化学性质相似;故A正确;
B、虽然两种元素的原子的最外层电子数相同,但它们的化学性质却不同.质子数为1的H元素,易得1个电子而形成最外层为2个电子的稳定结构;而质子数为11的原子最外层电子数为1,不稳定,易失最外层的1个电子形成稳定结构;故B不正确;
C、虽然两种元素的原子的最外层电子数相同,但它们的化学性质却完全不同.质子数为2的He为稀有气体元素,化学性质稳定;而质子数为12的原子最外层电子数为2,不稳定,易失最外层的2个电子形成稳定结构;故C不正确;
D、两种元素的原子电外层电子数分别为1和7,最外层电子数为1的Na元素易失去最外层电子,而最外层为7的Cl元素易得到电子;元素的化学性质不同,故D不正确.
故选A.
【点评】在原子的结构示意图中,最外层电子数能反映出其化学性质,一般最外层电子数相同即具有相似的化学性质,但要注意与特殊的元素区别开来.
14.亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒.区别它们的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种具有刺激性气味气体的是亚硝酸钠.该气体可能是()
A.NH3 B.SO2 C.NO2 D.N2
【分析】因为亚硝酸钠分解放出的有刺激性气味气体,所以该气体的元素组成必须不能超出亚硝酸钠中的元素组成,还要注意该气体有刺激性气味.
【解答】解:A、NH3中含有氢元素,而亚硝酸钠中没有氢元素,故A错误;
B、SO2中含有硫元素,而亚硝酸钠中不含有硫元素,故B错误;
C、NO2中的两种元素在亚硝酸钠中都有,并且该气体也是有刺激性气味的,故C正确;
D、N2是无色无味的气体,故D错误.
故选C.
【点评】由于该反应是分解反应,气体中所含的元素必须在亚硝酸钠中能找到,依据是反应前后元素种类不变.
15.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是()
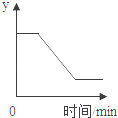
A.生成O2的质量 B.固体中MnO2的质量
C.固体中氧元素的质量 D.固体中钾元素的质量分数
【分析】根据图象可知,纵坐标表示的物质或元素开始不变,再逐渐减少,反应停止后不变,结合各物质即元素在反应中的变化情况来分析.
【解答】解:A.生成氧气的质量不断增加,不符合该图象.
B.二氧化锰在反应中为催化剂,反应前后质量不变,不符合该图象.
C、反应后生成氧气跑掉,故固体中氧元素的质量从开反应就不断减少,反应停止后不变,由于二氧化锰中也有氧元素,故最后不能为0,故符合该图象正确.
D.反应前后固体中钾元素的质量不变,固体质量减少,钾元素的质量分数增大,不符合该图象.
答案:C.
【点评】本题应用质量守恒的方法确定解答,解题关键明确图象含义和质量守恒定律的正确运用.
二、填空题:(共45分)
16.根据下列几种粒子的结构示意图,回答下列问题
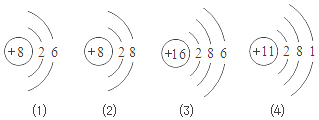
(1)其中属于阴离子是 (2) (填序号,下同);
(2)具有相似化学性质的是 (1)(3) ;
(3)属于同种元素的是 (1)(2) .(4)钠离子符号 Na+
(5)由氧原子变成氧离子发生的是 化学 变化,理由是 由原子变成离子,是在化学变化过程得电子 .
【分析】(1)阴离子的结构示意图中,核外电子数大于核内质子数;
(2)元素的化学性质决定于结构示意图中最外层电子数,最外层电子数相同的粒子则具有相似的化学性质;
(3)元素的种类决定于结构示意图中核内质子数,核内质子数相同的粒子属于同种元素;
(4)根据离子符号的写法写出钠离子符号;
(5)根据原子和离子的妆花分析回答.
【解答】解:(1)粒子(2)核内质子数为8而核外电子数为2+8=10,核外电子数大于质子数,为阴离子;故填:(2);
(2)粒子(1)、(3)最外层电子数均为6,因此这两种粒子的化学性质相似,都能表现出得到2个电子的性质;故填:(1)(3);
(3)粒子(1)与(2)核内均为个质子,质子数相同,属于同种元素;故填:(1)(2);
(4)钠离子符号为:Na+;故填:Na+;
(5)由氧原子变成氧离子发生的是化学变化,理由是由原子变成离子,是在化学变化过程得电子.故填:化学;原子变成离子,是在化学变化过程得电子.
【点评】正确区分粒子结构示意图的构成特点,明确元素种类及化学性质与粒子构成的相关联系,是解答此类问题所必然具备的知识基础.
17.某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
(1)甲同学选用如右图所示的装置制取氧气.
①写出仪器B的名称: 集气瓶 .
②甲同学应选取的试剂是Mn02和 H2O2 (填化学式),Mn02固体在该反应中起 催化 作用.
③除用排水法外,甲同学还可选择 向上排空气法 法收集氧气.
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现.该实验操作的目的是 检验装置的气密性 .
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为 2KMnO4![]() K2MnO4+MnO2+O2↑ .实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
K2MnO4+MnO2+O2↑ .实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2Mn04分解放出O2做出上述猜想的理由是 K2Mn04和MnO2都是含有氧元素的化合物 .
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后 测得Mn02的质量不变.则猜想 I 错误.
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得
出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 检验是否有氧气生成 .
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物K2O对其分 解产生影响.请设计实验方案验证: 取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系 .
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识? 必须通过认真分析,用实验来加以证明 .
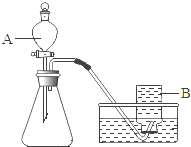
【分析】(1)熟悉常见仪器,了解名称;②根据反应装置和所提供药品,确定另一种药品;根据二氧化锰在反应中的表现了解作用;③根据氧气的密度和溶水性考虑收集方法;④实验前要检验装置的气密性;
(2)根据反应物、反应条件、生成物写出化学反应式;
【提出猜想】有氧气生成就要有氧元素存在;
【实验验证】要验证猜想II,可以用验证氧气的方法来确定氧气的有无,可以用带火星的木条深入收集的气体中,观察现象;
【拓展延伸】使两者形成对比,取等量的K2MnO4,其中一个加入K2O,另一个不加K2O,各自收集一瓶氧气,看所用的时间长短来确定,是否是K2O的影响;
【实验反思】总结实验的分析和解决过程,然后了解到需认真分析,并根据科学的方法去验
【解答】解:(1)图中B是集气瓶.
故答案为:集气瓶;
②如图装置适合固液不加热反应,我们可以用过氧化氢溶液和固体二氧化锰反应制取氧气,其中二氧化锰在反应前后性质和质量都不发生变化,所以二氧化锰起催化作用.
故答案为:H2O2、催化;
③因氧气的密度大于空气的密度,不易溶于水,所以除用排水法收集外,还可以用向上排空气法收集.
故答案为:向上排空气法;
④这种做法可以使装置内外形成压力差,看装置是否漏气.
故答案为:检验装置的气密性;
(2)加热高锰酸钾制取氧气的化学反应式是:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
故答案为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
【提出猜想】K2Mn04和MnO2都是含有氧元素的化合物,所以我们可以猜想有氧气生成.
故答案为:K2Mn04和MnO2都是含有氧元素的化合物.
【实验验证】①根据质量守恒定义和冷却后测得Mn02的质量不变可知,猜想I是错误的,故答案为:I;
②我们可以用验证氧气有无的方法去判断是否有氧气的生成,如用带火星的木条,深入收集的气体中,如果木条复燃说明有氧气生成.
故答案为:检验是否有氧气生成.
【拓展延伸】我们可以用如下实验验证:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
故答案为:取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
【实验反思】要想发现问题,必须细心认真;要想解决问题,必须认真分析问题的原因所在,并用实验去验证,故答案为:必须通过认真分析,用实验来加以证明.
答案:
(1)①集气瓶;
②H2O2、催化;
③向上排空气法;
④检验装置的气密性;
(2)2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
【提出猜想】K2Mn04和MnO2都是含有氧元素的化合物;
【实验验证】①I;②检验是否有氧气生成;
【拓展延伸】取等量的固体于两支试管中,一支试管中加入氧化钾,一支试管中不加氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集气体,收集一瓶氧气,所用时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
【实验反思】必须通过认真分析,用实验来加以证明.
【点评】本题考查制取氧气的实验以及相关问题,还有验证猜想的实验设计,要同学们具有综合的化学知识才可做好此题.
18.3月22日是“世界水日”.关于水的知识,请回答下列问题:
(1)下列净水方法中,生产自来水使用的方法有(填字母序号) ABE ;
A.沉淀B.过滤C.煮沸D.蒸馏E.吸附
(2)实验室常用过滤的方法对液体进行提纯,在此操作中需要用到的玻璃仪器有:玻璃棒、烧杯、 漏斗 (填仪器名称);生活中常用 煮沸 的方法将硬水软化.
(3)有关水的组成和结构的叙述中,正确的是(填字母序号) AD ;
A.水是由水分子构成的
B.水分子的相对分子质量是18g
C.水中氢、氧元素的质量比为2:1
D.水分子是由氢原子和氧原子构成的
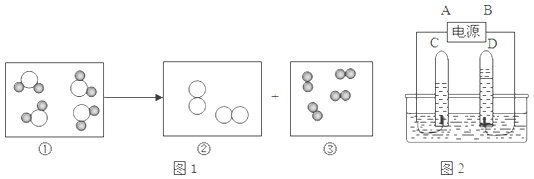
(4)下列图1示意图①~③中,“![]() ”表示氢原子,“
”表示氢原子,“![]() ”表示氧原子.表示化合物的是(填序号) ① ,③所代表的物质是图中 试管 C (填字母) 中产生的气体,图2中A是电源的 负 (填“正”或“负”)极.
”表示氧原子.表示化合物的是(填序号) ① ,③所代表的物质是图中 试管 C (填字母) 中产生的气体,图2中A是电源的 负 (填“正”或“负”)极.
(5)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,写出该反应的符号表达式 2H2O![]() 2H2↑+O2↑ .
2H2↑+O2↑ .
【分析】(1)根据常用净水方法回答;
(2)根据过滤所用仪器分析;生活中常用煮沸的方法将硬水中的钙、镁离子沉淀下来,达到软化水的目的;
(3)根据水的构成、组成,及相对分子质量和元素的质量比的相关知识分析解答;
(4)依据化合物分子中含有多种原子,电解水实验“负氢正氧、氢多氧少”进行回答;
(5)依据反应物、生成物、反应条件书写方程式.
【解答】解:(1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附;
(2)过滤需要的玻璃仪器有:烧杯、漏斗、玻璃棒;生活中常用煮沸的方法将硬水中的钙、镁离子沉淀下来,达到软化水的目的;
(3)A、水是由水分子构成的,正确;
B、水分子的相对分子质量是:2+16=18,单位是1,省略不写,故错误;
C、水中氢、氧元素的质量比为1×2:16=1:8,而不是2:1,故错误;
D、水分子是由氢原子和氧原子构成,正确;
(4)化合物是纯净物,所以化合物中只有一种分子,且分子中含有多种原子,分析图示中分子的情况可知构成化合物分子的是图①;③所代表的物质是由分子构成,是每个分子由两个氢原子构成的氢分子,氢分子构成氢气,氢气多,大约是氧气体积的2倍,是在负极得到的;
(5)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气,反应的化学方程式是:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
故答案为:
(1)ABE;(2)漏斗;煮沸;(3)AD;(4)①;C;负;(5)2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
【点评】本题考查知识较为综合,考查了水的净化、水的软化方法、水的电解等知识,掌握基础知识并结合题意逐一分析即可.
三、计算题:(共10分)
19.(10分)蛋白质在人体胃肠内与水反应,最终生成氨基酸被人体吸收.丙氨酸(化学式为C3H7O2N)就是其中的一种.请回答下列问题:
(1)丙氨酸分子中C、H、O、N各原子个数比为 3:7:2:1 .
(2)丙氨酸的相对分子质量是 89 ,氮元素的质量分数为 15.7% (计算结果精确到0.1%).
【分析】(1)根据丙氨酸分子的构成进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中元素的质量分数=![]() ×100%,进行分析解答.
×100%,进行分析解答.
【解答】解:(1)1个丙氨酸分子是由3个碳原子、7个氢原子、2个氧原子、1个氮原子构成的,丙氨酸分子中C、H、O、N的原子个数比为3:7:2:1.
(2)丙氨酸的相对分子质量为12×3+1×7+16×2+14=89.
氮元素的质量分数为![]() ×100%≈15.7%.
×100%≈15.7%.
故答案为:(1)3:7:2:1;(2)89;15.7%.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
2页

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...