由于格式问题此试题可能会出现乱码的情况
为了方便您阅读请点击右上角的全屏查看
2018石家庄市中考化学压轴试题
一.选择题
1.如图所示图标表示我国“国家节水标志”的是( )
A. B.
B. C.
C. D.
D.
2.下列有关化学符号“H2O”表示的意义,正确的是( )
A.水这种物质
B.水由氢原子和氧原子构成
C.一个水分子中含有一个氢分子
D.水由两个氢元素和一个氧元素组成
3.水是生命之源.下列关于水的说法不正确的是( )
A.水由液态变成气态时,分子间空隙变大
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成
C.活性炭具有吸附性,可用于除去水中的异味
D.如果将水样蒸干后有固体析出,这种水样中一定含有杂质
4.(石家庄中考化学)如图是电解水实验的装置图,下列说法错误的是( )

A.在水中加入少量氢氧化钠以增强导电性
B.反应一段时间后,a、b玻璃管中产生的气体体积比约为2:1
C.将燃着的木条分别放在两个玻璃管尖嘴口,打开活塞,a管的气体使燃着的木条燃的更旺,b管的气体被点燃
D.由电解水实验得出结论:水是由氢、氧两种元素组成的
5.小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,黏在烧杯上的塑料片脱落.加入的物质可能是( )
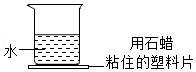
A.食盐 B.硝酸铵 C.硫酸铜 D.浓硫酸
6.如表是KCl和KNO3在不同温度下的溶解度.下列说法不正确的是( )
/℃ | 20 | 30 | 40 | 50 | |
溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO | 31.6 | 45.8 | 6.9 | 85.5 | |
A.20℃时,KCl的溶解度大于KNO3的溶解度
B.两种物质溶解度相等的温度在20~30℃之间
C.40℃时,5gKCl中加10g水可得33.3%溶液KNO3
D.50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出
7.下列有关溶液的说法正确的是( )
A.溶液均是无色的、透明的
B.可溶性物质溶于水时一定会放出热量
C.石灰水的溶质是石灰
D.溶液的均一性是指同一溶液各部分的性质、组成相同
8.25℃时向一定量不饱和KNO3溶液中逐渐加入KNO3固体,则下列图象中能正确表示此过程溶质质量变化规律的是( )
A. B.
B.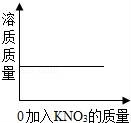 C.
C.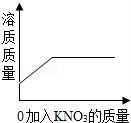 D.
D.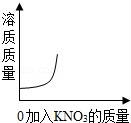
9.右图为固体物质X、Y的溶解度曲线.在温度为t2℃时分别把质量为a g的X、Y放入100g水中,下表为对溶液状态的判断以及使不饱和溶液达到饱和采取的措施.其中正确的是( )
| 状态 | 措施 |
A | X为饱和溶液,Y为不饱和溶液 | 给Y溶液加热蒸发适量的水 |
B | X为不饱和溶液,Y为饱和溶液 | 向X溶液加入固体X至有晶体残留 |
C | X、Y都是饱和溶液. | ﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣ |
D | X、Y都是不饱和溶液. | 把X溶液温度降低至t1℃,给Y溶液加热蒸发适量的水 |

A.A B.B C.C D.D
10.如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )

A.甲中混有少量杂质乙,可采用降温结晶的方法进行提纯
B.t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变
C.t2℃时,甲、丙溶液中溶质的质量分数甲>丙
D.t1℃时,60g水中溶解18g甲可得到其饱和溶液
二.(石家庄中考化学)填空与简答题
11.水在自然界、生产和生活中都有广泛用途.
(1)硬水和软水常用 来区分,软化硬水的方法很多,日常生活中常用 法
(2)在水的净化过程中,常利用 (填物质名称)的吸附性除去水中异味,高铁酸钾(化学式K2FeO4)是一种新型净水剂,可用于自来水净化处理,高铁酸钾中铁元素的化合价为 价.
(3)水是重要的溶剂,配制2%的氯化钠溶液500g,不需要使用的仪器是 (填写字母代号)
A.酒精灯 B.玻璃棒 C.烧杯 D.量筒 E.托盘天平
(4)除去NaOH溶液中混有的少量Na2CO3杂质,需加入适量的 溶液至不再产生沉淀为止,然后过滤,将滤液 得到NaOH固体.
(5)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO.一段时间后得到同温度的溶液乙;甲、乙溶液中溶质质量甲 乙(填“>、<、=”)
12.水是人类宝贵的资源.
(1)下列物质加入水中能形成溶液的是 ,能形成乳浊液的是 (填序号)
A.植物油 B.蔗糖 C.粉笔灰
(2)下列溶液pH>7的是 ,pH<7的是 (填序号)
A.食盐水 B.白醋 C.肥皂水
(3)NaCl溶于水,难溶于植物油;NaCl在热水中溶解的质量比在等质量的冷水中溶解的质量大.这说明,物质的溶解能力与 和 有关.
13.20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
组别 物质质量 | A | B | C | D | E |
NaCl晶体质量/g | 5 | 15 | 20 | 30 | 40 |
所得溶液质量/g | 105 | 115 | X | 130 | 136 |
请回答下列问题:
(1)A组的溶液为 (填“饱和”或“不饱和”)溶液.
(2)C组X的值为 .
(3)如图为NaCl的溶解度曲线图,图上a点纵坐标的值为 .Ca(OH)2的溶解度温度变化的趋势与NaCl相反,则室温时,向饱和石灰水加入少量生石灰,并恢复到室温,此时溶液中溶质的质量 (填“>”、“<”或“=”)原溶液中溶质的质量.
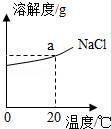
14.A、B、C 三个烧杯中盛有相同质量的水(其中A、C烧杯中水温为10℃,B烧杯中水温为30℃,不考虑溶解过程中温度的变化),分别加入甲、乙两物质各10g,充分溶解后所得现象如图1所示,试回答: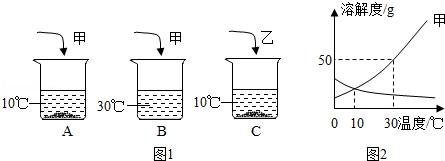
(1)你认为 烧杯中的溶液可能是不饱和溶液.
(2)如图2是甲、乙两种物质的溶解度曲线图,按图分析,10℃时A、C烧杯中未溶解的溶质质量关系是 (填“相等”或“不相等”).其它条件不变,将C烧杯中的温度升到30℃时,C烧杯中的溶液是 (填“饱和”或“不饱和”)溶液.
(3)若将A烧杯中的溶质全部溶解,可采用的方法有:
① ;② .
三.实验探究题
15.水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:

(1)图A实验中,铁钉锈蚀说明生锈是铁与 作用的结果.
(2)图B实验中,左边试管中收集到的气体是 ,检验该气体的方法是 .
(3)图C实验中,可观察到的现象是 ,若用pH试纸检测实验结果后集气瓶中水的pH应 7(填“小于”或“等于”或“大于”)
(4)40℃时,将50克KNO3充分溶于100克水中,形成KNO3溶液的质量是 克,若将溶液降温到20℃,溶液中溶质的质量分数是 .
16.如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
 (1)用图中序号表示配制溶液的正确操作顺序 .
(1)用图中序号表示配制溶液的正确操作顺序 .
(2)图②中用来取用NaCl的仪器是 .
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数位置见图⑥,则称取的NaCl质量为 g.
(4)NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的溶质质量分数 (填“大于”、“小于”或“等于”)10%.
四、计算应用题
17.在做电解水实验时,常在水中加入氢氧化钠来增强溶液的导电性,但氢氧化钠本身不会发生化学反应,质量也不会发生改变.现将含有8g氢氧化钠的水溶液109g通电一段时间后,生成1g氢气,请你计算(要有计算过程):
(1)电解所消耗的水的质量;
(2)电解水后的氢氧化钠溶液的质量分数.
石家庄中考化学参考答案与试题解析
一.选择题
1.如图所示图标表示我国“国家节水标志”的是( )
A. B.
B. C.
C. D.
D.
【考点】HH:几种常见的与化学有关的图标.
【分析】根据已有的化学图标的意义进行分析解答即可.
【解答】解:A、是剧毒品标志,错误;
B、是可循环塑料标志,错误;
C、是节约用水标志,正确;
D、是禁止放置易燃物标志,错误;
故选C.
2.(石家庄中考化学)下列有关化学符号“H2O”表示的意义,正确的是( )
A.水这种物质
B.水由氢原子和氧原子构成
C.一个水分子中含有一个氢分子
D.水由两个氢元素和一个氧元素组成
【考点】D1:化学式的书写及意义.
【分析】根据化学式的意义进行分析:①宏观意义:a.表示一种物质; b.表示该物质的元素组成; ②微观意义:a.表示该物质的一个分子; b.表示该物质的分子构成;据此进行分析解答.
【解答】解:A、化学符号“H2O”表示水这种物质,故选项说法正确.
B、水是由水分子构成的,水分子是由氢原子和氧原子构成,故选项说法错误.
C、分子是由原子构成的,一个水分子中含有2个氢原子,不含氢分子,故选项说法错误.
D、元素只讲种类、不讲个数,故选项说法错误.
故选:A.
3.水是生命之源.下列关于水的说法不正确的是( )
A.水由液态变成气态时,分子间空隙变大
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成
C.活性炭具有吸附性,可用于除去水中的异味
D.如果将水样蒸干后有固体析出,这种水样中一定含有杂质
【考点】71:电解水实验;BA:分子的定义与分子的特性;C6:碳单质的物理性质及用途.
【分析】根据水组成、电解水试验的现象和结论、水的净化等分析判断.
【解答】解:A、水由液态变成气态时,分子间空隙变大,故A说法正确;
B、电解水生成氢气和氧气,说明水是由氢元素和氧元素组成,故B说法不正确;
C、活性炭具有吸附性,可用于除去水中的异味,故C说法正确;
D、如果将水样蒸干后有固体析出,这种水样中一定含有杂质,故D说法正确.
故选B.
4.如图是电解水实验的装置图,下列说法错误的是( )

A.在水中加入少量氢氧化钠以增强导电性
B.反应一段时间后,a、b玻璃管中产生的气体体积比约为2:1
C.将燃着的木条分别放在两个玻璃管尖嘴口,打开活塞,a管的气体使燃着的木条燃的更旺,b管的气体被点燃
D.由电解水实验得出结论:水是由氢、氧两种元素组成的
【考点】71:电解水实验.
【分析】根据电解水试验的现象、结论、生成气体的性质和注意事项分析判断有关的说法.电解水时“正氧负氢,氢二氧一”.
【解答】解:A、由于氢氧化钠在水中能解离出自由移动的离子,在水中加入少量氢氧化钠以增强导电,故A说法正确;
B、由电解水的实验装置可知,反应一段时间后,a、b玻璃管中产生的气体体积比约为2:1,故B说法正确;
C、将燃着的木条分别放在两个玻璃管尖嘴口,打开活塞,a管的气体较多是氢气,具有可燃性,气体被点燃,b管的气体较少,是氧气,具有助燃性,使燃着的木条燃的更旺,故C说法错误;
D、电解水实验得出结论:水是由氢、氧两种元素组成的,故D说法正确.
故选C.
5.(石家庄中考化学)小琪往如图所示的烧杯中加入一种物质,轻轻搅拌后,黏在烧杯上的塑料片脱落.加入的物质可能是( )

A.食盐 B.硝酸铵 C.硫酸铜 D.浓硫酸
【考点】7F:溶解时的吸热或放热现象.
【分析】由于用石蜡粘住的塑料片脱落,说明加入物质在溶解或者反应过程中放热.有的物质溶于水时会放出热量,使溶液温度升高,如浓硫酸、氢氧化钠等;也可以是反应过程中是放热的,如氧化钙溶解于水和水反应.
【解答】解:A、食盐溶于水时,溶液温度变化不大,石蜡仍为固态,粘在烧杯上的塑料片不会脱落,故A错误;
B、硝酸铵溶于水时吸收热量,使溶液的温度降低,石蜡仍为固态,粘在烧杯上的塑料片不会脱落,故B错误;
C、硫酸铜溶于水时,溶液温度变化不大,石蜡仍为固态,粘在烧杯上的塑料片不会脱落,故C错误;
D、浓硫酸放入水中溶解时放出热量,使溶液温度升高,会使石蜡熔化,粘在烧杯上的塑料片脱落,故D正确.
故答案为:D
6.如表是KCl和KNO3在不同温度下的溶解度.下列说法不正确的是( )
/℃ | 20 | 30 | 40 | 50 | |
溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO | 31.6 | 45.8 | 6.9 | 85.5 | |
A.20℃时,KCl的溶解度大于KNO3的溶解度
B.两种物质溶解度相等的温度在20~30℃之间
C.40℃时,5gKCl中加10g水可得33.3%溶液KNO3
D.50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出
【考点】7P:晶体和结晶的概念与现象;7T:溶质的质量分数、溶解性和溶解度的关系.
【分析】A、根据20℃时,KCl溶解度是34g,KNO3的溶解度是31.6g进行分析;
B、根据图表中数据考虑进行分析;
C、根据40℃时,氯化钾的溶解度进行分析;
D、根据30℃时,硝酸钾的溶解度进行分析.
【解答】(石家庄中考化学)解:A、20℃时,KCl溶解度是34g,KNO3的溶解度是31.6g,所以20℃时,KCl溶解度大于KNO3的溶解度,故A正确;
B、在20~30℃之间,氯化钾从34g增加到37g,硝酸钾从31.6g增加到45.8g,所以两物质溶解度相等的温度在20~30℃之间,故B正确;
C、40℃时,氯化钾的溶解度是40g,所以10g水会溶解4g氯化钾,5gKCl加10g水可得到14g溶液,形成溶液的质量分数数是:![]() ×100%≈28.6%,故C错误;
×100%≈28.6%,故C错误;
D、30℃时,硝酸钾的溶解度45.8g,20g溶解硝酸钾为:45.8g×![]() =9.16g,所以50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出,故D正确..
=9.16g,所以50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出,故D正确..
故选:C.
7.下列有关溶液的说法正确的是( )
A.溶液均是无色的、透明的
B.可溶性物质溶于水时一定会放出热量
C.石灰水的溶质是石灰
D.溶液的均一性是指同一溶液各部分的性质、组成相同
【考点】7C:溶液的概念、组成及其特点;7D:溶液、溶质和溶剂的相互关系与判断;7F:溶解时的吸热或放热现象.
【分析】A、根据溶液的特点考虑;B、根据物质溶于水,能量的变化考虑;C、石灰水的溶质是氢氧化钙;D、根据溶液的均一性考虑.
【解答】解:A、溶液的特点:均一、稳定的混合物,溶液可以有颜色,例如硫酸铜溶液是蓝色,故A错;
B、物质溶于水,有的放热,有的吸热,例如:氢氧化钠溶于水放热,硝酸铵溶于水吸热,故B错;
C、石灰水的溶质是氢氧化钙,故C错;
D、溶液的均一性:是指同一溶液各部分的性质、组成相同,故D正确.
故选D.
8.25℃时向一定量不饱和KNO3溶液中逐渐加入KNO3固体,则下列图象中能正确表示此过程溶质质量变化规律的是( )
A. B.
B. C.
C.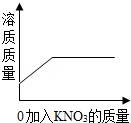 D.
D.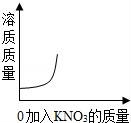
【考点】7D:溶液、溶质和溶剂的相互关系与判断;7J:饱和溶液和不饱和溶液相互转变的方法.
【分析】在一定温度下,在一定量的溶剂里,硝酸钾的溶解能力是有一定的限度的.
【解答】解:A、不饱和KNO3溶液中含有一定量的溶质硝酸钾;
B、向一定量不饱和KNO3溶液中逐渐加入KNO3固体时,硝酸钾能够继续溶解,直到达到饱和状态;
C、向一定量不饱和KNO3溶液中逐渐加入KNO3固体时,硝酸钾能够继续溶解,达到饱和状态时不再溶解;
D、在一定温度下,在一定量的溶剂里,硝酸钾不能无限溶解.
故选:C.
9.(石家庄中考化学)右图为固体物质X、Y的溶解度曲线.在温度为t2℃时分别把质量为a g的X、Y放入100g水中,下表为对溶液状态的判断以及使不饱和溶液达到饱和采取的措施.其中正确的是( )
| 状态 | 措施 |
A | X为饱和溶液,Y为不饱和溶液 | 给Y溶液加热蒸发适量的水 |
B | X为不饱和溶液,Y为饱和溶液 | 向X溶液加入固体X至有晶体残留 |
C | X、Y都是饱和溶液. | ﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣ |
D | X、Y都是不饱和溶液. | 把X溶液温度降低至t1℃,给Y溶液加热蒸发适量的水 |
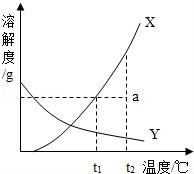
A.A B.B C.C D.D
【考点】7N:固体溶解度曲线及其作用;7I:饱和溶液和不饱和溶液;7J:饱和溶液和不饱和溶液相互转变的方法.
【分析】固体溶解度曲线上及上方的点表示的都是该固体物质的饱和溶液,而溶解度下方的点则表示的是该物质的不饱和溶液;根据固体物质的溶解度随温度变化的变化情况,可以判断出通过降温还是升温的方法使不饱和溶液变成饱和溶液.
【解答】解:A、由两物质的溶解度曲线可知,在t2℃时,X的溶解度大于ag,而Y的溶解度小于ag,因此质量为a g的X、Y放入100g水中,X溶液是不饱和溶液,而Y溶液是饱和溶液,且溶液中还有未溶解的溶质;故A错误;
B、由于X溶液在t2℃时是不饱和溶液,因此可以向溶液中添加溶质直至溶液达到饱和,故B正确;
C、由于X溶液是不饱和溶液,故C错误;
D、由于Y溶液是饱和溶液,故D错误;
故选B.
10.如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )
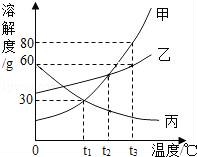
A.甲中混有少量杂质乙,可采用降温结晶的方法进行提纯
B.t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变
C.t2℃时,甲、丙溶液中溶质的质量分数甲>丙
D.t1℃时,60g水中溶解18g甲可得到其饱和溶液
【考点】7N:固体溶解度曲线及其作用;4H:结晶的原理、方法及其应用;7T:溶质的质量分数、溶解性和溶解度的关系.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:A、甲物质的溶解度受温度影响变化较大,所以甲中混有少量杂质乙,可采用降温结晶的方法进行提纯,故A正确;
B、t3℃时,将甲、丙的饱和溶液降温,甲物质的溶解度减小,析出晶体,乙物质的溶解度增大,所以甲溶液溶质的质量分数减小,丙不变,故B正确;
C、t2℃时,甲、丙溶液的状态不能确定,所以溶质的质量分数也不能确定,故C错误;
D、t1℃时,甲物质的溶解度是30g,所以60g水中溶解18g甲可得到其饱和溶液,故D正确.
故选:C.
二.填空与简答题
11.水在自然界、生产和生活中都有广泛用途.
(1)硬水和软水常用 肥皂水 来区分,软化硬水的方法很多,日常生活中常用 煮沸 法
(2)在水的净化过程中,常利用 活性炭 (填物质名称)的吸附性除去水中异味,高铁酸钾(化学式K2FeO4)是一种新型净水剂,可用于自来水净化处理,高铁酸钾中铁元素的化合价为 +6 价.
(3)水是重要的溶剂,配制2%的氯化钠溶液500g,不需要使用的仪器是 A (填写字母代号)
A.酒精灯 B.玻璃棒 C.烧杯 D.量筒 E.托盘天平
(4)除去NaOH溶液中混有的少量Na2CO3杂质,需加入适量的 氢氧化钙 溶液至不再产生沉淀为止,然后过滤,将滤液 蒸发结晶 得到NaOH固体.
(5)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO.一段时间后得到同温度的溶液乙;甲、乙溶液中溶质质量甲 > 乙(填“>、<、=”)
【考点】77:硬水与软水;4E:一定溶质质量分数的溶液的配制;4G:过滤的原理、方法及其应用;7M:固体溶解度的影响因素;8L:生石灰的性质与用途;9H:盐的化学性质;D6:有关元素化合价的计算.
【分析】(1)根据硬水和软水的区别方法及硬水软化的方法分析;
(2)根据活性炭的作用分析;根据化合物中元素正负化合价的代数和为零分析;
(3)根据配制溶液需要的仪器分析;
(4)根据碱和盐之间的反应及物质的分离方法分析;
(5)根据氧化钙吸收水份分析;
【解答】解:(1)生活中常用肥皂水来区分软水和硬水,加入肥皂水后振荡,泡沫丰富的是软水,泡沫少的是硬水;生活中常用加热煮沸的方法软化硬水;
(2)活性炭具有吸附性,常用于净水过程中吸收异味和色素;K2FeO4中钾元素为+1价,氧元素为﹣2价,设铁元素的化合价为a,则(+1)×2+a+(﹣2)×4=0,则a=+6;
(3)配制2%的氯化钠溶液500g,需要用到量筒量取水,用天平称量氯化钠,在烧杯里配制,用玻璃棒搅拌,不需要使用的仪器是酒精灯;
(4)除去NaOH溶液中混有的少量Na2CO3杂质,可以加入适量的氢氧化钙,因为氢氧化钙能与碳酸钠反应生成碳酸钙沉淀,从而除去碳酸根,并生成物氢氧化钠不带入新的杂质;用蒸发结晶的方法可以从滤液中得到氢氧化钠固体;
(5)因为20℃时Ca(OH)2的饱和溶液不会再溶解溶质,向其中加入CaO后,会吸收到一部分水份,使溶液中的溶剂减少,溶质会部分析出.所以得到的同温度的溶液乙中溶质的质量会小于原溶液中溶质的质量;
故答案为:(1)肥皂水;煮沸;(2)活性炭;+6;(3)A;(4)氢氧化钙;蒸发结晶;(5)>;
12.水是人类宝贵的资源.
(1)下列物质加入水中能形成溶液的是 B ,能形成乳浊液的是 A (填序号)
A.植物油 B.蔗糖 C.粉笔灰
(2)下列溶液pH>7的是 C ,pH<7的是 B (填序号)
A.食盐水 B.白醋 C.肥皂水
(3)NaCl溶于水,难溶于植物油;NaCl在热水中溶解的质量比在等质量的冷水中溶解的质量大.这说明,物质的溶解能力与 溶剂种类 和 温度 有关.
【考点】7G:悬浊液、乳浊液的概念及其与溶液的区别;7Q:物质的溶解性及影响溶解性的因素;99:溶液的酸碱性与pH值的关系.
【分析】(1)本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物;
(2)根据溶液的酸碱性与pH值的关系考虑;
(3)根据水和植物油属于溶剂种类不同,热水和冷水温度不同.
【解答】解:(1)在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物属于溶液,蔗糖易溶于水,形成均一、稳定的混合物,属于溶液;植物油不溶于水,与水混合形成乳浊液;
(2)白醋属于酸,pH<7;肥皂水显碱性,pH>7;
(3)水和植物油属于溶剂种类不同,热水和冷水温度不同;
故答案为:(1)B;A;(2)C;B;(3)溶剂种类;温度.
13.(石家庄中考化学)20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
组别 物质质量 | A | B | C | D | E |
NaCl晶体质量/g | 5 | 15 | 20 | 30 | 40 |
所得溶液质量/g | 105 | 115 | X | 130 | 136 |
请回答下列问题:
(1)A组的溶液为 不饱和 (填“饱和”或“不饱和”)溶液.
(2)C组X的值为 120 .
(3)如图为NaCl的溶解度曲线图,图上a点纵坐标的值为 36 .Ca(OH)2的溶解度温度变化的趋势与NaCl相反,则室温时,向饱和石灰水加入少量生石灰,并恢复到室温,此时溶液中溶质的质量 < (填“>”、“<”或“=”)原溶液中溶质的质量.

【考点】7I:饱和溶液和不饱和溶液;7N:固体溶解度曲线及其作用;8L:生石灰的性质与用途.
【分析】(1)根据题意可知A组中还能继续溶解氯化钠固体进行解答;
(2)根据氯化钠的溶解度随温度的升高而增大,20℃时100g水中能溶解20g氯化钠进行解答;
(3)根据题意可知,20℃时100g水中最多溶解36g氯化钠,氧化钙和水反应生成氢氧化钙进行解答.
【解答】解:(1)根据题意可知A组中还能继续溶解氯化钠固体,所以为不饱和溶液;故填:不饱和;
(2)氯化钠的溶解度随温度的升高而增大,20℃时100g水中能溶解20g氯化钠,所以C组X的值为100+20=120;故填:120;
(3)根据题意可知,20℃时100g水中最多溶解36g氯化钠,所以图上a点纵坐标的值为36,氧化钙和水反应生成氢氧化钙,向饱和石灰水加入少量生石灰,水的质量减少,并恢复到室温,此时溶液还是该温度的饱和溶液,所以所得溶液中溶质的质量小于原溶液中溶质的质量.故填:<.
14.A、B、C 三个烧杯中盛有相同质量的水(其中A、C烧杯中水温为10℃,B烧杯中水温为30℃,不考虑溶解过程中温度的变化),分别加入甲、乙两物质各10g,充分溶解后所得现象如图1所示,试回答:
(1)你认为 B 烧杯中的溶液可能是不饱和溶液.
(2)如图2是甲、乙两种物质的溶解度曲线图,按图分析,10℃时A、C烧杯中未溶解的溶质质量关系是 相等 (填“相等”或“不相等”).其它条件不变,将C烧杯中的温度升到30℃时,C烧杯中的溶液是 饱和 (填“饱和”或“不饱和”)溶液.
(3)若将A烧杯中的溶质全部溶解,可采用的方法有:
① 升温 ;② 加水 .
【考点】7I:饱和溶液和不饱和溶液;7J:饱和溶液和不饱和溶液相互转变的方法;7N:固体溶解度曲线及其作用.
【分析】(1)据图1的可得到答案;
(2)据溶解度曲线知10℃时甲、乙的溶解度相同解答;
(3)据甲的溶解度曲线知,甲的溶解度随温度的升高而增大.
【解答】解:(1)据图1的可知,A、C两个烧杯充分溶解后,溶质部分未溶解,B中全部溶解,故B烧杯中的溶液可能是不饱和溶液;
(2)有已知条件A、B、C 三个烧杯中盛有相同质量的水,10℃时甲、乙的溶解度相同,故分别加入甲、乙两物质各10g,充分溶解后A、C烧杯中未溶解的溶质质量关系是相等;由于乙的溶解度随温度的升高而减小,故其它条件不变,将C烧杯中的温度升到50℃时,C中会有新的晶体析出,故C烧杯中的溶液是饱和溶液;
(3)据甲的溶解度曲线知,甲的溶解度随温度的升高而增大,故若将A烧杯中的溶质全部溶解,可采用的方法有升高温度和增加溶剂水.
故答案为:(1)B;(2)相等;饱和;(3)①升温;②加水.
三.实验探究题
15.水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示回答下列问题:

(1)图A实验中,铁钉锈蚀说明生锈是铁与 氧气和水 作用的结果.
(2)图B实验中,左边试管中收集到的气体是 氧气 ,检验该气体的方法是 用带火星的木条靠近该气体,若木条复燃,则气体是氧气 .
(3)图C实验中,可观察到的现象是 发出明亮的蓝紫色火焰 ,若用pH试纸检测实验结果后集气瓶中水的pH应 小于 7(填“小于”或“等于”或“大于”)
(4)40℃时,将50克KNO3充分溶于100克水中,形成KNO3溶液的质量是 150 克,若将溶液降温到20℃,溶液中溶质的质量分数是 24% .
【考点】8G:金属锈蚀的条件及其防护;68:氧气的化学性质;71:电解水实验;7N:固体溶解度曲线及其作用;7R:溶质的质量分数.
【分析】(1)根据铁生锈的条件分析;
(2)电解实验中与正极相连的试管内的气体是氧气,根据氧气的助燃性进行检验;
(3)根据硫在氧气中燃烧的现象分析;
(4)根据溶液的质量=溶质的质量+溶剂的质量;根据20℃时溶液是饱和溶液分析.
【解答】(石家庄中考化学)解:(1)铁与水和氧气接触容易生锈,观察图示可知,铁钉锈蚀说明生锈是铁与氧气和水作用的结果;
(2)实验中,与正极相连的试管内的气体体积少,能使带火星的木条复燃,所以可以用带火星的木条靠近该气体,若木条复燃,则气体是氧气;
(3)硫在氧气中燃烧,发出明亮的蓝紫色火焰,放出大量的热,产生一种具有刺激性气味的气体二氧化硫,二氧化硫溶于水使水溶液呈酸性;
(4)溶液的质量=溶质的质量+溶剂的质量,所以40℃时,将50克KNO3充分溶于100克水中,形成KNO3溶液的质量是:100+50=150克;20℃时的溶解度是31.6克,若将溶液降温到20℃,溶液变成饱和溶液,有晶体析出,溶液中溶质的质量分数是:![]() ×100%=24%.
×100%=24%.
故答案为:(1)氧气和水;
(2)氧气;用带火星的木条靠近该气体,若木条复燃,则气体是氧气;
(3)发出明亮的蓝紫色火焰;小于;
(4)150;24%.
16.如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
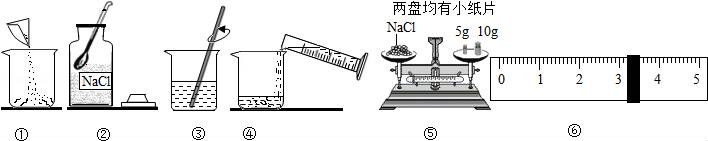 (1)用图中序号表示配制溶液的正确操作顺序 ②⑤①④③ .
(1)用图中序号表示配制溶液的正确操作顺序 ②⑤①④③ .
(2)图②中用来取用NaCl的仪器是 药匙 .
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数位置见图⑥,则称取的NaCl质量为 18.2 g.
(4)NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的溶质质量分数 小于 (填“大于”、“小于”或“等于”)10%.
【考点】4E:一定溶质质量分数的溶液的配制;43:称量器﹣托盘天平.
【分析】(1)根据已有的知识进行分析,配制溶液的步骤是计算、称量、溶解;可以据此解答该题;
(2)图②中的塑料仪器为药匙,可以据此解答该题;
(3)使用天平称取氯化钠的质量时,要将称量物放在左盘,砝码放在右盘,称量物的质量=砝码+游码;
(4)根据溶质质量分数公式可以求得溶液的质量,从而求得水的质量,再根据密度公式计算水的体积,砝码缺少一角则称量的食盐的质量减小,可以据此解答该题.
【解答】(石家庄中考化学)解:(1)称量食盐的质量首先打开广口瓶塞,倒放在桌面上,将取得的食盐放在天平的左盘,然后将称得的食盐放到烧杯中,再将量取的水倒入烧杯中,用玻璃棒搅拌使之溶解,故正确的顺序为②⑤①④③;
(2)图②中的塑料仪器为药匙;
(3)食盐的质量=砝码+游码,据图可知,砝码的读数是15g,游码的读数是3.2g,故食盐的质量=15g+3.2g=18.2g;(4)砝码缺少一角则称量的食盐的质量减小,溶质减少,则溶液变稀,溶质质量分数变小.
故答案为:(1)②⑤①④③;
(2)药匙;
(3)18.2g;
(4)小于.
四、计算应用题
17.在做电解水实验时,常在水中加入氢氧化钠来增强溶液的导电性,但氢氧化钠本身不会发生化学反应,质量也不会发生改变.现将含有8g氢氧化钠的水溶液109g通电一段时间后,生成1g氢气,请你计算(要有计算过程):
(1)电解所消耗的水的质量;
(2)电解水后的氢氧化钠溶液的质量分数.
【考点】G6:根据化学反应方程式的计算;7U:有关溶质质量分数的简单计算.
【分析】(1)根据反应的化学方程式,由产生氢气的质量可计算消耗水的质量;
(2)由于反应前后氢氧化钠质量不变,改变的只是溶液中水的质量,由氢氧化钠质量与所剩余溶液的质量比,可计算电解水后的氢氧化钠溶液的质量分数.
【解答】解:(1)设电解所消耗的水的质量为x
2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
36 4
x 1g
![]() =
=![]() x=9g
x=9g
(2)电解水后的氢氧化钠溶液的溶质的质量分数为:![]() ×100%=8%
×100%=8%
答:(1)电解所消耗的水的质量9g;
(2)电解水后的氢氧化钠溶液的质量分数8%.
第1页(共24页)

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...