各位同学在查看时请点击全屏查看
2017年六盘水中考化学试题
化学试题可能用到的相对原了质量:C 12 H l O 16 Ca 40 S 32 Al 27
一、选择题(本大题共8小题,每小题2分,共16分,在四个选项中只有一项符合题意,请把它选出来填涂在答题卡相应的位置)
1.奇妙的物质世界在不断变化,下列没有发生化学变化的是
A.光合作用 B.使用稀盐酸除铁锈 C.节日燃放礼花 D.白炽灯通电发光
2.下列实验操作正确的是

3.参加六盘水市夏季国际马拉松赛的运动员,剧烈运动后感觉肌肉酸胀,原因是人体产生了较多的乳酸(化学式为C3H6O3)。下列关于乳酸说法错误的是
A.乳酸属于有机物
B.乳酸由3个碳原子、6个氢原子和3个氧原子构成
C.乳酸中碳、氢、氧元素的质量比为6:1:8
D.乳酸中碳元素的质量分数为4O%
4.关于下列实验现象,描述错误的是
A.光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡
B.镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体
C.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
D.氢气在空气中燃烧,产生淡蓝色火焰,放出大量的热
5.对物质进行归类整理是化学学习的一种重要方法,下列归类关系正确的是
A.棉花、蚕丝、塑料——合成材料 B.纯碱、小苏打、硫酸铜——盐
C.氮气、氨气、臭氧——单质 D.水、干冰、氯酸钾——氧化物
6.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是
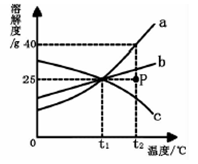
A. t1℃ 时,a、b、c饱和溶液的溶质质量分数为20%
B. P点表示:t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态
C. t2℃时,a、b、c三种物质溶液的溶质质量分数a>b>c
D. 7Oga的饱和溶液从t2℃降温到t1℃时,析出晶体15g
7.在“宏观一微观”之间建立联系,是学习化学学科必备的思维方式。下图是某反应的微观示意图,下列说法正确的是

A.该反应中甲、乙、丙、丁都属于化合物 B.反应生成丙、丁分子个数比为1:1
C.参加反应的甲、乙的质量比为6O: 224 D.该反应不遵守质量守恒定律
8.下图能正确反映其对应操作中各种量的变化关系的是

A.在碱溶液中加入一定量的稀盐酸,溶液pH的变化曲线
B.将等质量的铝粉和锌粉,分别放入质量分数相同的足量稀盐酸中
C.加热一定质量的氯酸钾和二氧化锰的混合固体,生成O2的质量与反应时间的关系
D. H2还原一定质量的CuO,固体的质量随反应时间的变化关系
二、填空题(本大题共5小题,每空l分,共17分)
9.(3分)请按要求用化学用语填空:
(l)氖气_______。
(2)二氧化硅中硅元素显+4 价_______。
(3)由两种原子团形成的化合物的化学式_______。
10.(4分)元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:

(l)溴的相对原子质量是_______。
(2)溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为:_______。
(4)若图二中C表示离子,则离子符号是_______。
11.(2分)目前人类可以从多方面获取能源,我国在能源获取方面取得较大突破。
(l)氢氧燃料电池是一种新型电池。氧气可从空气中获取,氢气可通过以下反应获取:
2NaCl+2H2O![]() 2X+Cl2↑+H2↑ 。其中X的化学式是_______。
2X+Cl2↑+H2↑ 。其中X的化学式是_______。
(2)截止2017年6月2日,我国在南海神狐海域连续开采可燃冰超过22天。可燃冰(化学式CH4·8H2O)能释放出甲烷气体,是未来洁净的新能源。请写出甲烷燃烧的化学方程式:_____。
12.(4分)水是人类的宝贵自然资源,与人类的生产、生活密切相关。
(l)饮用酸、碱性过强或硬度过大的水都不利于人体健康,可用______来测定水的酸碱度。
(2)检验水是硬水还是软水,可用的物质是______,日常生活中使硬水软化的方法是______。
(3)实验室用“电解水”或“氢气在氧气中燃烧”的实验探究水的组成元素,理论依据是______。
13.(4分)已知A~H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且c能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据如图所示的转化关系(图中反应条件均已略去),请回答:
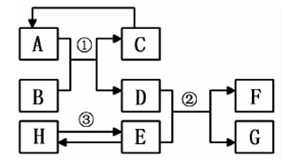
(l)写出物质B的化学式:_________。
(2)写出序号对应的化学方程式:①_________。②_________。
(3)反应③的基本反应类型是_________。
三、实验与探究(本大题共3小题,每空l分,共18分)
14.(7分)下图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题:
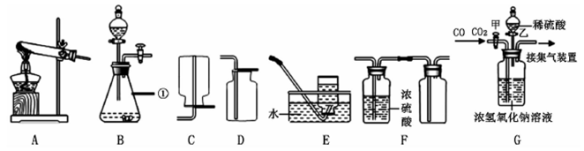
(l)图中标识① 仪器的名称是:_______。
(2)用A装置制取氧气的化学方程式为:_______。
(3)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:_______。(在A一E中选),用该装置制取CO2的化学方程式为:_______。
(4)若用F装置收集一瓶干燥的某气体,则该气体可能是_______。(填字母代号)
A.NH3 B.H2 C.O2 D.CH4
(5)工业上常需分离CO、CO2的混合气体。某同学采用装置G也能达到分离该混合气体的目的,操作步骤如下:
① 关闭活塞乙,打开活塞甲,通入混合气体,可收集到_______气体;② 然后,_______(填操作),又可收集到另一种气体。
15.(7分)甲、乙两名同学分别做了碳酸钠溶液与氢氧化钡溶液反应的实验,反应后都进行过滤得到无色滤液,他们对自己得到的无色滤液中溶质的成分进行探究。请你一同参与他们的探究活动
【提出猜想】他们各自所得滤液中溶质的成分有如下几种可能:
A.NaOH B.Na2CO3、Ba(OH)2、NaOH C. _______ D. Na2CO3和NaOH
【讨论交流】上述猜想中,肯定不成立的是_____(填猜想序号),其理由是_____。
【实验探究】甲、乙两同学为了验证各自所得滤液的成分,分别进行了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
甲同学 | 取少量滤液于试管中,加入足量的_____溶液 | _____ | 滤液中溶质的成分与猜想C对应 |
乙同学 | 取少量滤液于试管中,加入足量的Na2CO3溶液 | 无明显实验现象 | 滤液中溶质的成分与猜想A 对应 |
【反思与评价】经过讨论,大家一致认为甲同学的实验结论是正确的,乙同学的实验结论不一定正确。请你帮乙同学设计实验,进一步确定乙同学得到的滤液中溶质的成分。
实验操作及实验现象 | 实验结论 |
_________ | 滤液中溶质的成分与猜想_____对应 |
16.(4分)某化学兴趣小组进行了识别化肥的探究活动,他们对氯化铵、碳酸氢铵、硫酸钾、磷矿粉四种化肥进行了如下探究:
(l)取上述四种化肥各少量分别放入试管观察,从外观上即可与其他化肥以别出来的是_____。
(2)在装有另外三种化肥的试管中,分别加入少量稀盐酸,有气体产生的是_____。
(3)若要想继续区别出另外两种化肥,选用的物质是_____。,现象和结论_____。
四、化学与生活(本大题共1小题,每空l分,共4分)
17.(4分)化学无处不在,小到日常生活,大到航空航天。
(l)日常生活中,炒菜油锅着火时,用锅盖盖灭用此方法灭火的原理是:_____。
(2)端午节人们食用粽子纪念屈原使用糯米、食盐、火腿瘦肉、少量油作为某种粽子的原料,从营养均衡的角度看,你认为还缺少的营养素为:_____。
(3)2017年5月,我国首款大型客机C919首飞成功。C919结构上多处运用钛合金和铝锂合金作为零件,钛合金和铝锂合金属于_____材料。
(4)近年来,我国各地都在建设湿地公园,湿地可以调节气候条件、改善环境、净化水源。请你提出一条净化湿地水源的合理化建议:_____。
五、计算题(本大题共l小题,共5分)
18.(5分)水钢采用烟气脱硫工艺,不仅能消除二氧化硫,防止形成酸雨,还能将其转化为硫酸钙等产品,实现“变废为宝”。反应的化学方程式为:2CaCO3+ O2+ 2SO2![]() 2CaSO4+2CO2,现用2.5t含碳酸钙80%的石灰石吸收烟气中的二氧化硫。求:
2CaSO4+2CO2,现用2.5t含碳酸钙80%的石灰石吸收烟气中的二氧化硫。求:
(l)石灰石中碳酸钙的质量______;
(2)可吸收二氧化硫的质量(要求有计算步骤)。
2017年六盘水中考化学试题参考答案
1.D 2.C 3.B 4.A 5.B 6.A 7.C 8.B
9.(1)Ne;(2)![]() ;(3)(NH4)2SO4/NH4NO3/NH4HCO3/(NH4)2CO3;
;(3)(NH4)2SO4/NH4NO3/NH4HCO3/(NH4)2CO3;
10.(1)79.90;(2)B;(3)KBr;(4)S2-;
11.(1)NaOH;(2)CH4+2O2![]() CO2+2H2O
CO2+2H2O
12.(1)pH试纸/pH计/酸度计;(2)肥皂水,加热/煮沸;(3)化学反应前后元素种类不变/质量守恒定律。
13.(1)Fe2O3;(2)①3CO+Fe2O3![]() 2Fe+3CO2;②Fe+CuCl2=FeCl2+Cu/Fe+Cu(NO3)2=Fe(NO3)2+Cu;
2Fe+3CO2;②Fe+CuCl2=FeCl2+Cu/Fe+Cu(NO3)2=Fe(NO3)2+Cu;
(3)复分解反应。
14.(1)锥形瓶;(2)2KMnO4![]() K2MnO4+MnO2+O2↑/2KClO3
K2MnO4+MnO2+O2↑/2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)BD/BE;CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)C;(5)①CO;②关闭活塞甲,打开活塞乙。
15.【提出猜想】C.Ba(OH)2、NaOH;
【讨论交流】B;Na2CO3和Ba(OH)2能发生反应/Na2CO3和Ba(OH)2不能共存/Na2CO3+Ba(OH)2=2NaOH+BaCO3↓
【实验探究】
实验操作 | 实验现象 | 实验结沦 |
Na2CO3溶液 | 产生白色沉淀/溶液变浑浊 | 猜想C成立 |
K2CO3溶液 | 产生白色沉淀/溶液变浑浊 | 猜想C成立 |
Na2SO4溶液 | 产生白色沉淀/溶液变浑浊 | 猜想C成立 |
K2SO4溶液 | 产生白色沉淀/溶液变浑浊 | 猜想C成立 |
稀硫酸 | 产生白色沉淀/溶液变浑浊 | 猜想C成立 |
答案合理均给分 | ||
【反思与评价】
实验操作及实验现象 | 实验结沦 |
加入Ba(OH)2溶液或Ca(OH)2溶液,无明显现象 | 与猜想A对应 |
加入BaCl2溶液或CaCl2溶液,无明显现象 | 与猜想A对应 |
加入稀盐酸或稀硫酸,无明显现象 | 与猜想A对应 |
答案合理均给分 | |
加入Ba(OH)2溶液或Ca(OH)2溶液,产生白色沉淀 | 与猜想D对应 |
加入BaCl2溶液或CaCl2溶液,产生白色沉淀 | 与猜想D对应 |
加入稀盐酸或稀硫酸,产生大量气泡 | 与猜想D对应 |
答案合理均给分 | |
16.(l)磷矿粉;(2)碳酸氢铵/NH4HCO3
(3)熟石灰【Ca(OH)2】;固体研磨产生刺激性气味的是氯化铵,另一个是硫酸钾/硝酸银(AgNO3);溶液产生白色沉淀的是氯化铵,另一个是硫酸钾/氯化钡(BaCl2);溶液产生白色沉淀的是硫酸钾,另一个是氯化铵/氢氧化钡【Ba(OH)2】;固体研磨产生刺激性气味的是氯化铵,另一个是硫酸钾/氢氧化钡【Ba(OH)2】;溶液产生刺激性气味的是氯化铵,产生白色沉淀的是硫酸钾(合理均给分)
17.(l)隔绝氧气(空气);(2)维生素;(3)金属;
(4)植树造林/泥沙过滤污染物/污水处理达标再排放/活性炭吸附/明矾沉降(合理均给分)
18. (1)2t;(1分)(2)1.28t
![]()

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...