请点击全屏查看
2018黄石市中考化学模拟试题
请用下列物质的字母填空,完成1-4题
A.氖气 B.二氧化硫 C.高锰酸钾 D.红磷
![]() 1.进入空气中能形成酸雨的是( );
1.进入空气中能形成酸雨的是( );
2.可用于军事上做烟幕弹的是( );
3.常用于充入霓虹灯的是( );
4.常用于实验室制取氧气的是( );
5.根据日常经验和你所学的化学知识,判断下列变化中不属于化学变化的是( )
A.灯泡发光 B.燃放烟花 C.金属生锈 D.动物的呼吸作用
6.(2018黄石化学)以下物质![]() 的用途,利用其物理性质的是( )
的用途,利用其物理性质的是( )
A.氮气填充食品包装袋 B.氧气供给呼吸
C.中暑后用酒精擦拭降温 D.石灰水检验二氧化碳
7.下列实验操作正确的![]() 是( )
是( )
A. ![]()

![]() B.
B. 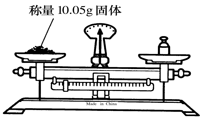
C. 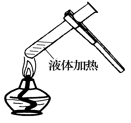 D.
D. 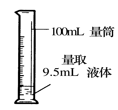
8. 雾霾是一种大气污染现象,下列不属于雾霾治理措施的是( )
A.植树绿化,![]() 美化环境 B.外出时佩戴防雾霾口罩
美化环境 B.外出时佩戴防雾霾口罩
C.提倡绿色出行,发展公共交通 D.减少燃煤发电,增加太阳能发电
9. 下列关于空气成分的说法正确的是( )
A.稀有气体在通电时能发出不同颜色的光 B.氧气的化学性质比较活泼,易燃烧
C.二氧化碳有毒,含量增多会引起温室效应 D.氮气约占空气体积的21%
10. 下列有关实验现象的![]() 描述正确的是( )
描述正确的是( )
A.硫在空气中燃烧产生蓝紫色火焰 B.木炭在氧气中燃烧生成白色固体
C.铁丝在空气中燃烧火星四射生成四氧化三铁 D.磷在空气中燃烧产生大量白烟
11. 我国自主研制的首艘货运飞船“天舟一号”已于 2017年4月20日发射成功,并与天宫二号空间实验室完成交会对接。本次使用的是长征七号遥二运载火箭,火箭采用了液氧煤油发动机等新技术。下列说法不正确的是( )
A.液氧是助燃剂 B.液氧是混合物 C.煤油是燃料 D.煤油有可燃性
12. (2018黄石化学)下列是李明在实验室进行氧气的制取、收集、验满和验证性质的操作,其中合理的是( )
A.将高锰酸钾放于试管口向上的![]() 试管中进行加热
试管中进行加热![]() 分解
分解
B.将导管口伸到集气瓶的瓶口处,用向下排空气法收集氧气
C.将点燃的木条伸入集气瓶中进行验满
D.将镁条伸入充满氧气的![]() 集气瓶中并点燃,验证氧气的性质
集气瓶中并点燃,验证氧气的性质
13.分别取两份相同质量、相同浓度的过氧化氢溶液,其中一份(用a表示)直接制取氧气,在另一份(用b表示)中加入少量的二氧化锰。下列图像正确的是( )
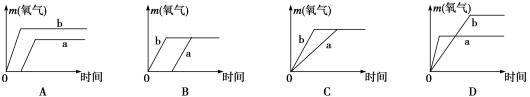
14.分析、推理和类比是化学学习中常用的思维方法,下列分析、推理或类比正确的是( )
A.物质与氧发生的反应属于氧化反应,所以有氧气参加的反应一定是氧化反应
B.化学变化都伴随有能量变化,所以发光放热的一定是化学变化
C.二氧化锰能加快过氧化氢的分解速率,所以催化剂一定能加快反应速率
D.分解反应有多种生成物,所以有多种物质生成的都是分解反应
42.(2018黄石化学)一辆汽车,发动机的输出功率是29.4kW,热机效率为20%,它带有16kg汽油,如果车匀速直线运动的速度为60km/h,(汽油的热值为4.6×107J/kg)
问:(1)汽油完全燃烧放出的热量;
(2)汽车所受的阻力;(3)汽车能行驶多远。
43.(6分![]() )空气是一种重要的自然资源,请选择适当的化学用语填空:
)空气是一种重要的自然资源,请选择适当的化学用语填空:
(1)工业上生产氮肥的重要原料是________;
(2)鱼虾能在水中生存,说明水中含有________;
(3)脆的饼干长时间暴露在空气中会变软是因为空气中有________;
(4)工业上常根据沸点不同利![]() 用分离________________的方法得到氧气,此
用分离________________的方法得到氧气,此![]() 过程是________变化;
过程是________变化;
(5)为了安全,我们用________取代氢气来充灌探空气球和飞艇。
44.(2018黄石化学)(6分)写出下列反应的文字表达式并回答相关问题:
(1)淡黄色粉末物质在氧气中燃烧,![]() 发出明亮的蓝紫色火焰: ;此反应类型属于: ;
发出明亮的蓝紫色火焰: ;此反应类型属于: ;
(2)一种黑色固体在氧气中燃烧,其生成物可使澄清石灰水变浑浊: ![]() ;
;
(3)铁丝在氧气里燃烧 。为了防止熔化物溅落下来使集气瓶炸裂,应当在瓶内预先放少量 ;
(4)实验室用纯净物制取氧气的反应: 。
45.(6分)含碳燃料(煤、液化石油气、天然气等)在缺氧时不完全燃烧会生成一种大气污染物一氧化碳,一氧化碳是一种无色、无味的剧毒气体,难溶于水,密度比空气略小,它在空气中点燃完全燃烧时,生成二氧化碳。请回答:
(1)上述信息中,属于一氧化碳气体物理性质的是______________________________;化学性质有_______![]() ________________________________;若要收集一氧化碳气体最合适的收集方法是_______________;
________________________________;若要收集一氧化碳气体最合适的收集方法是_______________;
(2)写出一氧化碳在空气中完全燃烧的文字表达式:![]() ___________________________,其完全燃烧的产物在空气中含量过高会引起_______________效应,根据题目所给信息,你认为家中的燃气热水器_________(填能或不能)装在浴室内。
___________________________,其完全燃烧的产物在空气中含量过高会引起_______________效应,根据题目所给信息,你认为家中的燃气热水器_________(填能或不能)装在浴室内。
46.(6分)某紫黑色固体加热后可得固体粉末A和B以及气体C,A与白色粉末D共热生成C和E,其中A在该反应前后的质量和化学性质都不变,若将细铁丝放在C中点燃,燃烧剧烈,火星四射,生成黑色固体F。
根据以上实验事实,写出下列物质的名称:
A. _________B. _________C. _________D. _________E. _________ F. _________
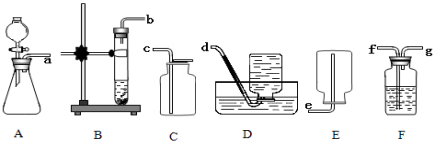
47.(6分)实验室制取气体时所需的一些装置如图所示,请回答下列问题:
(1)实验室用过氧化氢溶液和二氧化锰![]() 混合制取氧
混合制取氧![]() 气的文字表达式为_____________;可选择的发生装置有__________(填字母);选择气体收集方法时,气体的下列性质:①颜色;②密度;③溶解性;④可燃性;⑤是否与水或空气的成分反应,必须考虑的是________(填序号)。
气的文字表达式为_____________;可选择的发生装置有__________(填字母);选择气体收集方法时,气体的下列性质:①颜色;②密度;③溶解性;④可燃性;⑤是否与水或空气的成分反应,必须考虑的是________(填序号)。
(2)MnO2在该反应中可以重复使用,理由是__________________________________。
(3)已知F装置中盛有浓硫酸(浓硫酸有吸水性),现要收集一瓶干燥的氧气,所选择装置的玻璃管的连接顺序为___________(填字母),若将F装置装满水来收集氧气,则气体应从______管通入。
48.(2018黄石化学)(6分)“化学反应条件的控制是实验的灵魂”。某探究小组发现若反应过快,产生的气体不易及时收集,为探究影响过氧化氢溶液分解快慢的因素,于是进行了如下探究:
【提出问题】过氧化氢溶液分解快慢与哪些因素有关呢?
【猜想与假设】猜想一:可能与过氧化氢的浓度有关;
猜想二:可能与 有关;
猜想三:可能与是否用催化剂有关。
【设计并实验】该探究小组用不同浓度的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧![]() 气体积和反应所需时间,记录数据如下表.
气体积和反应所需时间,记录数据如下表.
实验 序号 | 过氧化氢 的浓度 | 过氧化氢溶液 体积(mL) | 温度 | 二氧化锰 的用量/g | 收集氧气 的体积/ml | 反应所需 的时间/s |
① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30% | 5 | 35 | 0 | 2 | 49.21 |
④ | 30% | 5 | 55 | 0 | 2 | 10.76 |
【收集证据】要比较不同浓度的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是 (选填“实验序号”)。由实验③和④对比可知,化学反应速率与温度的关系是: 。
【解释与结论】
(1)通过探究,了解控制过氧化氢分解快慢的方法,现用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量 。(填“减小”、“增大”或“不变”)
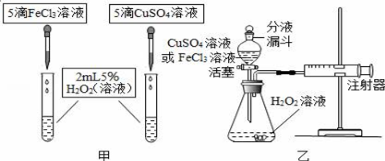
(2)为比较相同浓度的FeCl3(氯化铁)溶液和CuSO4(硫酸铜)溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
【定性研究】如图甲,可通过观察___________来定性比较两者的催化效果.
【定量研究】如图乙,要定量比较两者的催化效果,可测量生成等体积气体所需的______.

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...