各位同学在查看时请点击全屏查看
2018年晋中中考化学模拟试题
可能用到的相对原子质置:
K一39 C一12 N一14 O一16 Cl一35.5 Na一23 Ca一40
第I卷(选择题共16分)
一、化学模拟试题选择题(下列各题只有一个正确选项。其中1~4小题各1分,5~10题各2分。本大题共16分)
 1.右图是某菜农使用化肥包装袋上的部分说明,该化肥属于()
1.右图是某菜农使用化肥包装袋上的部分说明,该化肥属于()
A.氮肥B.磷肥C.钾肥D.复合肥料
2.生活离不开化学。下列做法中合理的是
A.青少年适量补充微量元素铁以预防佝偻病
B.利用硝酸铵溶于水吸热的原理,自制冰袋给发烧病人降温
C.为了节约粮食,把霉变大米淘净后继续食用
D.食用甲醛浸泡的海产品,可提高人体免疫力
3.取3枚洁净无锈的铁钉,分别加入3支试管中,如图所示的物质进行实验,试管中 铁钉锈蚀速度由快到慢的顺序为()
铁钉锈蚀速度由快到慢的顺序为()
A.①②③B.②①③
C.②③①D.③①②
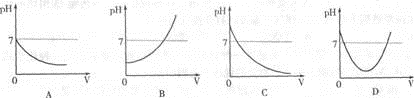
4.在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色。在上述过程中,表示溶液的pH(纵坐标)与滴加乙溶液的体积V(横坐标)之间的关系的正确图像是()
5.人类从石器时代进入铜器时代,继而进入铁器时代,铜作为金属材料一直被广泛应用着。下面冶炼铜的方法中,利用了置换反应的是:
①C+2CuO![]() 2Cu+CO2↑ ②CO+CuO
2Cu+CO2↑ ②CO+CuO![]() Cu+CO2
Cu+CO2
③H2 + CuO==== Cu + H2O ④Fe + CuSO4 =Cu + FeSO4
A.①②③ B.①③④ C.②③④ D.①②
6.下列推论正确的是()
A. 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.酸与碱反应生成盐和水,所以生成盐和水反应一定是酸与碱的反应
C.燃烧都伴随着发光、放热,所以有发光、放热现象的就是燃烧
D.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
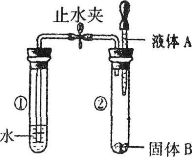 7.如右图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的()
7.如右图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的()
A.水和浓硫酸 B.水和生石灰
C.水和氢氧化钠 D.水和氯化钠
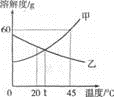 8.甲、乙两种固体物质的溶解度曲线如右图。下列说法正确的是()
8.甲、乙两种固体物质的溶解度曲线如右图。下列说法正确的是()
A.甲物质的溶解度为60 g
B.t ℃时,甲、乙两物质的溶解度相等
C.升高温度可使不饱和的甲溶液变为饱和溶液
D.t ℃乙物质的饱和溶液降到20 ℃时,溶液中溶质质量分数增大。
9.为得到纯净的物质,某同学设计下表中的除杂方法其中方法正确的是( )
| 物质 | 所含杂质 | 除去杂质的方法 |
A | NaCl溶液 | Na2C03 | 加人稀硫酸至不再产生气泡 |
B | Cu0粉末 | C | 加入过量稀盐酸,充分反应 |
C | N2气体 | 02 | 将气体缓缓通过灼热的铜网 |
D | KCl溶液 | CuCl2 | 加入氢氧化钠溶液至不再产生沉淀 |
10.某兴趣小组为探究活泼金属与酸反应的规
![]()
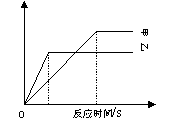 律,将质量相等的甲、乙两种金属分别放入到质量
律,将质量相等的甲、乙两种金属分别放入到质量
分数相同的足量稀盐酸中,经实验测定并绘制出生
成氢气的质量与反应时间的关系(见右图)。分析
图像得到的以下结论中,一定正确的是:
A.金属甲比金属乙活泼
B.金属甲比金属乙的相对原子质量大
C.金属乙比金属甲的反应速率大
D.金属乙比金属甲的化合价高
第Ⅱ卷(非选择题共34分)
二、填空与简答(共18分)
1.(4分)用符号或化学式填空:
① 2个亚铁离子 ②一种有机物
③ 氢氯酸 ④正二价的锰元素
2.(4分) 把生锈的铁钉放在足量的稀盐酸中,可以看到的现象是
、 。
涉及的化学方程式是_________________________、 。
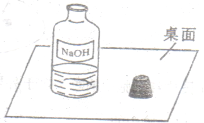 3.(5分)一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如右图)。
3.(5分)一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如右图)。
(1)此情此景你首先想到的是它可能变质了,该变质反应的化学方程式为:
(2)围绕此瓶NaOH溶液是否变质的问题,她们利用实验室现有的几种种试剂(氯化钙溶液、氢氧化钙溶液、稀盐酸、石蕊试液、酚酞试液等)展开了探究活动。
①小娟取少量溶液于试管中,滴加某种试剂,有气泡产生,由此证明NaOH溶液已经变质。
你认为小娟所加的试剂是 。小丽取少量溶液于试管中,滴加几滴酚酞试液,看到溶液呈红色,由此来说明NaOH溶液已变质。你认为她的检验方法是否成功?理由是 。
②小娟欲除去变质的溶液中的杂质,请你帮助小娟完成以下探究方案:取变质溶液于烧杯中,逐渐加入 试剂,并不断振荡,至不再产生 为止,再进行过滤操作,即可得到NaOH溶液,反应的化学方程式为: 。
4.(5分)同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案。请你和他们一起完善下表的探究方案并回答有关问题。
(1)填表
实验步骤 | 观察到的现象 |
① 在试管中取少量盐酸,插入铁丝,充分作用。 |
|
② 在①所得的溶液中,插入 ,充分作用。 | 无明显现象 |
③ 在②所得的溶液中插入 ,充分作用。 |
|
结论:金属活动性Al > Fe > Cu
(2)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论。小华要补充的实验是 。
三、实验与探究(共10分)
5、(4分)向某氢氧化钠溶液中加入一定量的稀硫酸。反应结束后,小明、小芳两位同学欲探究“氢氧化钠和硫酸是否恰好完全反应”,他们设计了如下实验,请你和他们一起完成:
| 实验操作 | 实验现象 | 结论 |
小明 | 用玻璃棒蘸取反应后的溶液滴在pH试纸上,并与标准比色卡对比。 | pH__________。 | 恰好完全反应。 |
小芳 | (1)取反应后的少量溶液于试管中,加入镁条; | (1)___________________; | (1)硫酸已完全反应。 |
(2)再取反应后的少量溶液于另一支试管中,滴加_____________溶液。 | (2)___________________。 | (2)氢氧化钠已完全反应。 |
6.(6分)下图是实验室制备物质的常用装置,根据装置回答:
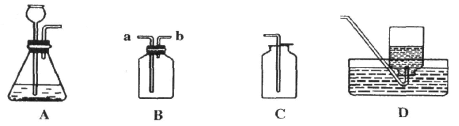
① 可用装置A制取的气体有
②装置C可用于收集中① 气体,
装置D可用于收集中① 气体
装置B可用于收集中① 气体。
③若用装置B除去二氧化碳中少量的水蒸气,可在装置中装入 ,气体应从 端进入。
四、计算与应用(共6分)
7.作物的无土栽培可以显著提高产品的产量和质量。某茄子的无土栽培营养液中含有7.08%的KNO3。
(1)KNO3中氮、氧元素的质量比为 。
(2)要配制150kg该营养液,需要KNO3的质量 kg。
8.用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠。为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品3.3g,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如右图所示。求:
(1)该纯碱样品中碳酸钠的质量分数。(精确到0.1%)
(2)所加入氯化钙溶液的溶质质量分数。
2018年晋中中考化学模拟试题参考答案
第一卷 选择题(共16分)
1---5 DBBCB 6---10 DDCCC
第二卷 非选择题(共34分)
二.填空与简答(每空一分,共18分)
1. 略
2.铁锈溶解,生成黄色溶液;有气泡冒出;Fe2O3 + 6HCl= 2FeCl3+ 3H2O
Fe + 2HCl= FeCl2 + H2↑
3.⑴CO2 + 2NaOH = Na2CO3 + H2O
⑵①稀盐酸; NaOH溶液 、 Na2CO3溶液均显碱性,都能使酚酞试液呈红色
②氢氧化钙溶液;沉淀; Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH
4.①冒出气泡;②铜丝;③铝丝;铝丝表面覆盖一层黑色物质
⑵铜丝和稀盐酸的反应
三.实验与探究(共10分)
5.PH=7;无明显现象;酚酞试液;溶液不变红
6.① H2、O2、CO2 (答出两种气体既可) ② CO2 O2 CO2 (答出一种气体既可)③ 浓硫酸 a
四.计算与应用(共6分,7题2分,8题4分)
7.⑴ 7:24 ⑵ 10。62
8.解:设该纯碱样品中碳酸钠的质量为x,22.2g氯化钙溶液中溶质的质量为y,则
Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
106 111 100
x y 3.0g
![]() 解之得:x=3.18(g),y=3.33(g)
解之得:x=3.18(g),y=3.33(g)
所以,该纯碱样品中碳酸钠的质量分数为:![]() =96.4%
=96.4%
所加入氯化钙溶液的溶质质量分数为:![]() =15%
=15%
第 5 页 共 5 页

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...