各位同学在查看时请点击全屏查看
2018年阳泉市中考化学模拟试题
一、化学模拟试题选择题
1.下列生活用品中,属于纯净物的是()
A.牛奶 B.冰水 C.加铁酱油 D.山西陈醋
2.下列厨房用品加到水中不能形成溶液的是()
A.面粉 B.料酒 C.食盐 D.白糖
3.豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指()
A.原子 B.分子 C.元素 D.单质
4.吸烟时,烟气中能与血红蛋白结合引起中毒的物质是()
A.氧气 B.氮气 C.一氧化碳 D.二氧化碳
5.下列实验操作正确的是()
A. 熄灭酒精灯 B.
熄灭酒精灯 B. 倾倒液体
倾倒液体
C.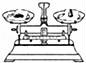 称量固体 D.
称量固体 D. 过滤
过滤
6.锂电池在手机和电脑中被广泛使用.在元素周期表中,锂元素的信息如图所示,对图中信息解释不正确的是()
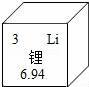
A.原子序数为3 B.锂原子的核外电子数为3
C.元素符号为Li D.锂原子的质量为6.94g
7.百合具有润肺止咳、养颜美容等功效,百合中含有秋水仙碱,其化学式为C22H25NO6,下列说法中正确的是()
A.秋水仙碱由碳、氢、氧三种元素组成
B.一个秋水仙碱分子由22个碳原子、25个氢原子、1个氮原子和3个氧分子构成
C.秋水仙碱分子中碳、氢、氮、氧原子个数比为22:25:1:6
D.秋水仙碱中氢元素的质量分数最大
8.化学对环境的保护和改善起着重要作用,下列做法错误的是()
A.工业废水经处理达标后再排放
B.高炉炼铁的废气直接排放到大气中
C.推广秸秆综合利用,杜绝露天焚烧
D.低碳生活倡导乘坐公交车、骑自行车、步行等出行方式
9.物质的组成和结构决定性质,性质决定用途.下列叙述正确的是()
A.干冰升华吸热,可用于人工降雨
B.汽油含有乳化剂,可以除去油污
C.煤、石油、天然气都有可燃性,可大量用作燃料
D.生铁坚硬,可以作医疗手术器械
10.下列图象能正确反映对应变化关系的是()
|
|
|
|
A.向一定量的MnO2中加入H2O2溶液 | B.加热一定量的高锰酸钾固体 | C.向一定量的硝酸银溶液中加入铜粉 | D.向两份完全相同的盐酸中加入镁和锌 |
A.A、 B.B、 C.C、 D.D、
二、生活生产应用题(化学方程式每空2分,其余每空1分,共11分)
11.水是人类宝贵的自然资源,在生活生产中用途较广.根据下列有关水的叙述,用适当的化学用语填空:
水通电可生成,在该变化过程中不发生改变的是;向水中通入二氧化碳则生成,水还是重要的溶剂,氯化钠溶液中的溶质为.
12.(7分)在牙膏中,常用轻质碳酸钙粉末作摩擦剂,生产轻质碳酸钙主要流程如下:
![]()
(1)生石灰主要成分为(填化学式),反应②属于(填“吸热”或“放热”)反应.
(2)“操作Ⅰ”中的操作是,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有.
(3)反应③的化学方程式.
(4)反应①的化学反应类型是.
三、阅读理解题(化学方程式每空2分,其余每空1分,共13分)
13.(10分)学习化学使我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.
(1)我们身边有各种各样的物质,例如氧气、金刚石、乙醇、铁、高锰酸钾等,他们都是由不同微粒构成的,请选择上述物质填空阅读下列科普短文.

依据文章内容,回答下列问题:
(1)空气中形成酸雨的主要气体是.
(2)SO2与SO3、NO与NO2组成元素相同,但化学性质不同,其原因是.
(3)保护环境,减少酸雨,人人有责,作为一名公民,我们可采取的措施是.
四、活动探究题(化学方程式每空2分,其余每空1分,共20分)
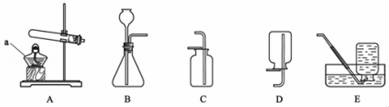
15.(10分)老师为同学们提供了如下实验装置:

(1)写出图中带有标号的仪器名称:a;B装置中长颈漏斗须伸入液面下的原因是.
(2)实验室制取气体时均应先;实验室制取CO2的常用药品是.有关反应的化学方程式为,应选用的发生装置和收集装置是(填字母代号),检验二氧化碳是否集满的方法是;证明集气瓶内的气体是二氧化碳,应该进行的操作和现象是.
(3)将长颈漏斗换成分液漏斗就能制取另一种气体,写出制取该气体的化学方程式.
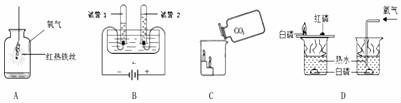
16.下面是研究氧气的性质,水的组成,二氧化碳的性质,燃烧条件的实验,根据图示,回答问题.

(1)实验A中铁丝在氧气中燃烧,反应的化学方程式为.
(2)实验B得出的结论是.
(3)实验C说明二氧化碳具有的性质是.
(4)实验D是通过控制哪些因素来探究可燃物燃烧的条件.
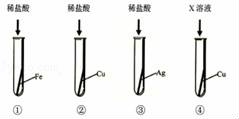
17.实验课上,化学老师拿来铁、铜、银三种金属,要求同学们设计实验探究它们的活动性顺序.
(1)一组同学做了如图①②③三个实验,未能去确定其活动性顺序,原因是,小明提出再补充实验④,就可验证这三种金属的活动性顺序,则实验④中的X溶液为.
(2)二组同学认为上述四个实验中实验(填序号)可以不做,就能判断出三种金属的活动性顺序.
(3)三组同学认为改用另外三种药品也可验证出铁、铜、银的活动性顺序,这三种药品是.
五、定量分析题(共6分)
18.(6分)在实验室里加热30g氯酸钾和二氧化锰的混合物制取氧气,加热至不再产生气体为止,称量剩余固体质量为20.4g,请计算.
(1)生成氧气的质量为g;
(2)固体剩余物中氯化钾的质量.
(3)回收固体混合物中二氧化锰的步骤是:.
2018年阳泉市中考化学试题参考答案
一、选择题
1.下列生活用品中,属于纯净物的是()
A.牛奶 B.冰水 C.加铁酱油 D.山西陈醋
【考点】纯净物和混合物的判别.
【分析】本题考查利用纯净物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子.
【解答】解:牛奶中含有蛋白质、油脂等物质,属于混合物,故A错;
B、冰水是由水一种物质组成,属于纯净物,故B正确;
C、加铁酱油中含有色素、含铁元素的物质,氯化钠等物质,属于混合物,故C错;
D、山西陈醋中含有醋酸和水等物质,属于混合物,故D错.
故选B.
【点评】在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成
2.下列厨房用品加到水中不能形成溶液的是()
A.面粉 B.料酒 C.食盐 D.白糖
【考点】溶液的概念、组成及其特点.
【分析】本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物.
【解答】解:A、面粉不溶于水,与水混合形成悬浊液,故A正确;
B、料酒易溶于水形成均一稳定的混合物,属于溶液,故B错;
C、食盐易溶于水形成均一稳定的混合物,属于溶液,故C错;
D、白糖易溶于水形成均一稳定的混合物,属于溶液,故D错;
故选A.
【点评】应熟悉溶液是一种均一稳定的混合物,在不改变条件时,溶液的组成和浓度都不会发生变化,要与悬浊液和乳浊液区分.
3.豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指()
A.原子 B.分子 C.元素 D.单质
【考点】元素的概念.
【分析】豆类、动物肝脏中含有丰富的“铁和锌”不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
【解答】解:豆类、动物肝脏中含有丰富的“铁和锌”,主要是以无机盐的形式存在,不是以单质、分子、原子等形式存在,这里所指的“铁和锌”是强调存在的元素,与具体形态无关.
故选C.
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.
4.吸烟时,烟气中能与血红蛋白结合引起中毒的物质是()
A.氧气 B.氮气 C.一氧化碳 D.二氧化碳
【考点】烟的危害性及防治.
【分析】A、氧气时供给人类呼吸的物质,不会有毒;
B、氮气是大气的主要成分之一,无毒;
C、一氧化碳能与人体的血红蛋白结合,使人中毒;
D、二氧化碳随不供给人类呼吸,但无毒.
【解答】解:A、氧气时供给人类呼吸的气体,能与血红蛋白结合,但不会引起中毒,故错误;
B、氮气是大气的主要成分,不会与血红蛋白结合引起中毒,故错误;
C、一氧化碳容易与血液中的血红蛋白结合,使人中毒,故正确;
D、二氧化碳虽然不能供给呼吸,但无毒,故错误.
故选C
【点评】此题是生活实际型题型,考查我们身边的化学,了解与生活有关的化学知识,知道一氧化碳的性质,了解吸烟的危害,杜绝吸烟.
5.下列实验操作正确的是()
A. 熄灭酒精灯 B.
熄灭酒精灯 B. 倾倒液体
倾倒液体
C. 称量固体 D.
称量固体 D. 过滤
过滤
【考点】加热器皿﹣酒精灯;称量器﹣托盘天平;液体药品的取用;过滤的原理、方法及其应用.
【分析】A、根据酒精灯的使用方法进行分析判断;
B、根据液体药品的取用方法进行分析判断;
C、根据托盘天平使用时的注意事项去分析判断;
D、根据过滤的方法进行分析判断.
【解答】解:A、熄灭酒精灯要用灯帽盖灭,不能用嘴吹灭,图中所示操作错误;
B、取用液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨;图中所示操作错误;
C、称量氯化钠固体时,要放在纸上称量,图中所示操作正确;
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、图中所示操作错误.
故选:C.
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.
6.锂电池在手机和电脑中被广泛使用.在元素周期表中,锂元素的信息如图所示,对图中信息解释不正确的是()

A.原子序数为3 B.锂原子的核外电子数为3
C.元素符号为Li D.锂原子的质量为6.94g
【考点】元素周期表的特点及其应用.
【分析】依据锂的最外层电子数判断其所属元素的种类,依据元素中期表中所示的信息的意义分析解答即可.
【解答】解:A、由图示可知锂的原子序数为3,故正确;
B、锂原子的核外电子数=质子数=3,故正确;
C、由图示可知锂元素的元素符号为Li,故正确;
D、图示中的6.941指的是锂的相对原子质量,单位不是克,故错误;
故选:D.
【点评】了解元素周期表的特点及其应用,核外电子在化学反应中的作用是解题的关键所在.
7.百合具有润肺止咳、养颜美容等功效,百合中含有秋水仙碱,其化学式为C22H25NO6,下列说法中正确的是()
A.秋水仙碱由碳、氢、氧三种元素组成
B.一个秋水仙碱分子由22个碳原子、25个氢原子、1个氮原子和3个氧分子构成
C.秋水仙碱分子中碳、氢、氮、氧原子个数比为22:25:1:6
D.秋水仙碱中氢元素的质量分数最大
【考点】化学式的书写及意义;元素的质量分数计算.
【分析】A.根据物质的组成来分析;
B.根据物质的分子结构来分析;
C.根据物质的化学式来分析;
D.根据化合物中某元素质量的计算方法来分析.
【解答】解:A.秋水仙碱的化学式为C22H25NO6,可见它是由碳、氢、氮、氧四种元素组成的,故错误;
B.秋水仙碱的化学式为C22H25NO6,可见一个秋水仙碱分子中有22个碳原子、25个氢原子、1个氮原子和6个氧原子,故错误;
C.秋水仙碱的化学式为C22H25NO6,可见其中碳、氢、氮、氧原子个数比为22:25:1::6,故正确;
D.秋水仙碱的化学式为C22H25NO6,其中碳元素的质量为:12×22=264;氢元素的质量为1×25=25;氮元素的质量为14;氧元素的质量为16×6=96,可见其中碳元素的质量分数最大,故错误.
故选:C.
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
8.化学对环境的保护和改善起着重要作用,下列做法错误的是()
A.工业废水经处理达标后再排放
B.高炉炼铁的废气直接排放到大气中
C.推广秸秆综合利用,杜绝露天焚烧
D.低碳生活倡导乘坐公交车、骑自行车、步行等出行方式
【考点】水资源的污染与防治;防治空气污染的措施.
【分析】A、根据工业废水经处理达标后再排放可以防止水污染解答;
B、根据高炉炼铁的废气直接排放到大气中,易造成空气污染解答;
C、根据推广秸秆综合利用,杜绝露天焚烧,可以防止空气污染解答;
D、根据乘坐公交车、骑自行车、步行等出行方式可以减少二氧化碳的排放进行解答.
【解答】解:
A、工业废水经处理达标后再排放可以防止水污染,故正确;
B、高炉炼铁的废气直接排放到大气中,易造成空气污染,故错误;
C、推广秸秆综合利用,杜绝露天焚烧,可以防止空气污染,故正确;
D、乘坐公交车、骑自行车、步行等出行方式可以减少二氧化碳的排放,故正确.
答案:B
【点评】本题是对所学知识的总结题,平时学习知识时一定要严密,要多总结多练习.化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,是中考热点之一,在学习过程中要理论联系实际,在实践中领会知识,运用所学知识去解决实际问题.
9.物质的组成和结构决定性质,性质决定用途.下列叙述正确的是()
A.干冰升华吸热,可用于人工降雨
B.汽油含有乳化剂,可以除去油污
C.煤、石油、天然气都有可燃性,可大量用作燃料
D.生铁坚硬,可以作医疗手术器械
【考点】溶解现象与溶解原理;二氧化碳的用途;生铁和钢;化石燃料及其综合利用.
【分析】A.根据二氧化碳的用途来分析;
B.根据溶解原理来分析;
C.根据燃料燃烧对环境的影响来分析;
D.根据生铁易锈蚀来分析.
【解答】解:A.干冰升华吸热可用于人工降雨,是利用了干冰升华吸热的性质,故正确;
B.汽油可以溶解油污,所以可以清除油污,故错误;
C.大量燃烧煤炭和石油作燃料会产生大量的污染物,造成空气的污染,故错误;
D.生铁接触到空气和水易发生锈蚀,制造医疗手术器械应该用不锈钢,故错误.
故选A.
【点评】本题考查的知识点较多,但是难度并不大,需要加强基础知识的记忆.
10.下列图象能正确反映对应变化关系的是()
|
|
|
|
A.向一定量的MnO2中加入H2O2溶液 | B.加热一定量的高锰酸钾固体 | C.向一定量的硝酸银溶液中加入铜粉 | D.向两份完全相同的盐酸中加入镁和锌 |
A.A、 B.B、 C.C、 D.D、
【考点】金属的化学性质;催化剂的特点与催化作用;质量守恒定律及其应用.
【分析】A、二氧化锰在过氧化氢分解的过程中作催化剂,反应前后质量不变.
B、高锰酸钾分解产生了氧气,反应后锰元素的质量分数发生了改变.
C、根据铜与硝酸银反应溶液质量的变化考虑;
D、根据氢元素的质量守恒来进行判断;
【解答】解:A、二氧化锰在过氧化氢分解的过程中作催化剂,反应前后质量不变,图象应成一条水平直线,故图象与实验操作过程不对应.
B、高锰酸钾分解产生了氧气,使固体的总质量减少,虽然锰元素的质量不变,但反应前后锰元素的质量分数应增大,完全分解后不变,图象应该是先上升后成一条水平直线,故图象与实验操作过程不对应.
C、铜与硝酸银反应生成银和硝酸铜,方程式为Cu+2AgNO3═Cu(NO3)2+2Ag.由于进入溶液的铜的相对质量小于置换出来的银的相对质量,所以溶液质量减少,反应完毕,溶液质量不变了,故图象与实验操作过程对应.
D、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故图象与实验操作过程不对应.
故选:C.
【点评】本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.
二、生活生产应用题(化学方程式每空2分,其余每空1分,共11分)
11.水是人类宝贵的自然资源,在生活生产中用途较广.根据下列有关水的叙述,用适当的化学用语填空:
水通电可生成 H2、O2 ,在该变化过程中不发生改变的是 H、O ;向水中通入二氧化碳则生成 H2CO3 ,水还是重要的溶剂,氯化钠溶液中的溶质为 NaCl .
【考点】化学符号及其周围数字的意义.
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
【解答】解:水在通电的情况下生成氢气和氧气,其化学式分别为:H2、O2;
化学变化的实质是旧分子分裂成原子,原子重新组合成新分子,故化学过程中不变的是氢原子和氧原子,其符号分别为:H、O;
向水中通入二氧化碳,二氧化碳与水反应生成碳酸,碳酸的化学式为:H2CO3;
氯化钠溶液中的溶质是氯化钠,其化学式为:NaCl;
故答案为:H2、O2 H、O H2CO3 NaCl
【点评】本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.
12.在牙膏中,常用轻质碳酸钙粉末作摩擦剂,生产轻质碳酸钙主要流程如下:
![]()
(1)生石灰主要成分为 CaO (填化学式),反应②属于 放热 (填“吸热”或“放热”)反应.
(2)“操作Ⅰ”中的操作是 过滤 ,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有 漏斗 .
(3)反应③的化学方程式 CO2+Ca(OH)2══CaCO3↓+H2O .
(4)反应①的化学反应类型是 分解反应 .
【考点】碳酸钙、生石灰、熟石灰之间的转化;过滤的原理、方法及其应用;生石灰的性质与用途;物质发生化学变化时的能量变化;书写化学方程式.
【分析】(1)根据生石灰是氧化钙,氧化钙与水反应生成氢氧化钙的同时放出热量;(2)根据不溶于液体的固体和液体分离的方法和用到的仪器考虑;(3)氢氧化钙与二氧化碳反应生成碳酸钙和水,碳酸钙后面标上沉淀符号;(4)根据反应物是一种,生成物是两种回答本题.
【解答】解:(1)生石灰是氧化钙化学式是CaO;氧化钙与水反应生成氢氧化钙的同时放出热量;
(2)不溶于液体的固体和液体分离的方法是过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗;
(3)反应物是二氧化碳和氢氧化钙,生成物是碳酸钙和水,碳酸钙后面标上沉淀符号,所以方程式是:CO2+Ca(OH)2══CaCO3↓+H2O;
(4)反应物是一种,生成物是两种,属于分解反应.
(1)CaO;放热;(2)过滤;漏斗;(3)CO2+Ca(OH)2══CaCO3↓+H2O;(4)分解反应.
【点评】该题是以工业生产流程为情景题,通过读图,联系课本相关知识即可顺利完成,了解方程式的写法和反应基本类型的特点.
三、阅读理解题(化学方程式每空2分,其余每空1分,共13分)
13.(10分)(2017•盂县一模)学习化学使我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.
(1)我们身边有各种各样的物质,例如氧气、金刚石、乙醇、铁、高锰酸钾等,他们都是由不同微粒构成的,请选择上述物质填空(2017•盂县一模)阅读下列科普短文.

依据文章内容,回答下列问题:
(1)空气中形成酸雨的主要气体是 SO2、NO2、NO .
(2)SO2与SO3、NO与NO2组成元素相同,但化学性质不同,其原因是 分子构成不同 .
(3)保护环境,减少酸雨,人人有责,作为一名公民,我们可采取的措施是 减少使用煤、石油等化石燃料 .
【考点】酸雨的产生、危害及防治.
【分析】(1)二氧化硫与氮的氧化物能与水反应,生成硫酸、硝酸,溶液呈酸性,是造成酸雨的主要气体,据此进行分析解答;
(2)根据分子构成回答;
(3)根据酸雨的成因回答.
【解答】解:(1)形成酸雨的主要气体是SO2、NO2、NO;
(2)SO2和SO3、NO和NO2组成元素相同,但分子不同,所以化学性质不同;
(3)减少酸雨主要是减少二氧化硫的排放,如出行时,多乘公共交通工具等;
故答案为:(1)SO2、NO2、NO (2)分子构成不同
(3)减少使用煤、石油等化石燃料
【点评】本题考查酸雨的形成过程,通过对酸雨形成的了解,可以使我们更好的了解如何防止酸雨.
四、活动探究题(化学方程式每空2分,其余每空1分,共20分)
15.(10分)(2017•盂县一模)老师为同学们提供了如下实验装置:
(1)写出图中带有标号的仪器名称:a 酒精灯 ;B装置中长颈漏斗须伸入液面下的原因是 防止生成的气体从长颈漏斗逸出 .
(2)实验室制取气体时均应先 检查装置气密性 ;实验室制取CO2的常用药品是 大理石(或石灰石)与稀盐酸 .有关反应的化学方程式为 CaCO3+2HCl=CaCl2+CO2↑+H2O ,应选用的发生装置和收集装置是 BC (填字母代号),检验二氧化碳是否集满的方法是 把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满 ;证明集气瓶内的气体是二氧化碳,应该进行的操作和现象是 向集气瓶中倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,证明集气瓶内的气体是二氧化碳 .
(3)将长颈漏斗换成分液漏斗就能制取另一种气体,写出制取该气体的化学方程式 2H2O2![]() 2H2O+O2↑ .
2H2O+O2↑ .
【考点】二氧化碳的实验室制法;二氧化碳的检验和验满;书写化学方程式.
【分析】(1)要熟悉各种仪器的名称、用途和使用方法;
B装置中长颈漏斗须伸入液面下,这样能够防止生成的气体从长颈漏斗逸出;
(2)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大,不能燃烧,不支持燃烧;
把气体通入澄清石灰水中,如果澄清石灰水变浑浊,说明是二氧化碳;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气.
【解答】解:(1)a是酒精灯;
B装置中长颈漏斗须伸入液面下能够防止生成的气体从长颈漏斗逸出.
故填:酒精灯;防止生成的气体从长颈漏斗逸出.
(2)实验室制取气体时均应先检查装置气密性;
实验室制取CO2的常用药品是大理石(或石灰石)与稀盐酸;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
碳酸钙和稀盐酸反应不需要加热,应该用B装置作为发生装置;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
检验二氧化碳是否集满的方法是:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满;
证明集气瓶内的气体是二氧化碳,应该进行的操作和现象是:向集气瓶中倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,证明集气瓶内的气体是二氧化碳.
故填:检查装置气密性;大理石(或石灰石)与稀盐酸;CaCO3+2HCl=CaCl2+CO2↑+H2O;BC;把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满;向集气瓶中倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,证明集气瓶内的气体是二氧化碳.
(3)将长颈漏斗换成分液漏斗就能制取另一种气体氧气,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2↑.
2H2O+O2↑.
故填:2H2O2![]() 2H2O+O2↑.
2H2O+O2↑.
【点评】本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.
16.下面是研究氧气的性质,水的组成,二氧化碳的性质,燃烧条件的实验,根据图示,回答问题.
(1)实验A中铁丝在氧气中燃烧,反应的化学方程式为 3Fe+2O2![]() Fe3O4 .
Fe3O4 .
(2)实验B得出的结论是 水是由氢元素和氧元素组成的 .
(3)实验C说明二氧化碳具有的性质是 不能燃烧、不能支持燃烧、密度比空气的大 .
(4)实验D是通过控制哪些因素来探究可燃物燃烧的条件 可燃物是否与氧气(或空气)接触,可燃物是否达到燃烧所需的温度 .
【考点】燃烧与燃烧的条件;氧气的化学性质;二氧化碳的物理性质;二氧化碳的化学性质;电解水实验.
【分析】(1)根据铁丝在氧气中燃烧,生成四氧化三铁解答;
(2)根据电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2解答;
(3)根据蜡烛由下至上依次熄灭解答.
(4)根据物质燃烧的条件分析,物质燃烧的条件是:物质具有可燃性、与氧气接触、达到着火点.
【解答】解:(1)铁丝在氧气中燃烧,生成四氧化三铁,反应的化学方程式为:3Fe+2O2![]() Fe3O4;
Fe3O4;
(2)根据电解水时,正极产生的是氧气,负极产生的是氢气,可得水是由氢元素和氧元素组成的.
(3)C实验的实验现象是蜡烛由下至上依次熄灭,可得二氧化碳的密度比空气大,不能燃烧,不支持燃烧,
(4)实验D中,水中的白磷与氧气隔绝,铜片上的白磷和红磷的着火点不同,故通过控制可燃物是否与氧气接触、温度是否达到可燃物的着火点的方法探究燃烧的条件.
故答案为:(1)3Fe+2O2![]() Fe3O4;
Fe3O4;
(2)水是由氢元素和氧元素组成的;
(3)不能燃烧、不能支持燃烧、密度比空气的大; (4)可燃物是否与氧气(或空气)接触,可燃物是否达到燃烧所需的温度.
【点评】电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的,同时说明在化学变化中,分子可分,原子不可分.
17.实验课上,化学老师拿来铁、铜、银三种金属,要求同学们设计实验探究它们的活动性顺序.
(1)一组同学做了如图①②③三个实验,未能去确定其活动性顺序,原因是 Cu、Ag均不与盐酸反应,无法比较两者的活动性顺序 ,小明提出再补充实验④,就可验证这三种金属的活动性顺序,则实验④中的X溶液为 AgNO3溶液 .
(2)二组同学认为上述四个实验中实验 ③ (填序号)可以不做,就能判断出三种金属的活动性顺序.
(3)三组同学认为改用另外三种药品也可验证出铁、铜、银的活动性顺序,这三种药品是 Fe、CuSO4溶液、Ag(或FeSO4溶液、Cu、AgNO3溶液) .

【考点】金属活动性的探究.
【分析】在金属活动性顺序中,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,要比较金属的活动性大小,常用金属与盐溶液的反应.要验证三种金属活动性大小关系时,通常采取“三取中”的方法即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.
【解答】解:(1)一组同学做了如图①②③三个实验,未能确定其活动性顺序的原因是:铜、银都不与盐酸反应,再补充实验④利用铜与硝酸银的反应,就可验证出这三种金属的活动性顺序,所以实验④中的X溶液为AgNO3溶液.
(2)通过①可以说明铁位于氢的前边,通过②可以说明铜位于氢的后边,通过④可以说明铜比银活泼,上述实验③可以不做,也能判断出三种金属的活动性顺序.
(3)三组同学认为改用三种药品也可验证出铁、铜、银的活动性顺序,可以利用“三取中”的方法,选用的药品是:铁、硫酸铜、银或硫酸亚铁、铜、硝酸银.
故答为:(1)Cu、Ag均不与盐酸反应,无法比较两者的活动性顺序,AgNO3溶液;(2)③;(3)Fe、CuSO4溶液、Ag(或FeSO4溶液、Cu、AgNO3溶液).
【点评】本题主要考查了对金属活动性顺序的应用和理解,难度不是很大,通过练习,培养学生的理解能力和应用能力.
五、定量分析题(共6分)
18.在实验室里加热30g氯酸钾和二氧化锰的混合物制取氧气,加热至不再产生气体为止,称量剩余固体质量为20.4g,请计算.
(1)生成氧气的质量为 9.6 g;
(2)固体剩余物中氯化钾的质量.
(3)回收固体混合物中二氧化锰的步骤是: 溶解、过滤、洗涤、干燥 .
【考点】根据化学反应方程式的计算.
【分析】根据质量守恒定律可知试管内物质质量的减少量就是生成的氧气的质量,根据方程式由氧气的质量,列比例式计算出参加反应的氯酸钾和氯化钾的质量即可,MnO2不溶于水,KCl溶于水,以此来解答.
【解答】解:(1)由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧气:30g﹣20.4g=9.6g;
故填:9.6;
(2)设生成氯化钾的质量为x
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
149 96
x 9.6g
![]()
x=14.9g
答:反应后剩余固体中氯化钾的质量为14.9g;
(3)充分反应后混合物含KCl、MnO2,MnO2不溶于水,KCl溶于水,从剩余物中回收干燥的二氧化锰,则溶解、过滤、洗涤、干燥.
故答案为:(1)9.6;(2)14.9g;
(3)溶解、过滤、洗涤、干燥.
【点评】做本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量进行进一步计算.

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...